Disolventes en la Industria Química/Texto completo
Este wikilibro está siendo desarrollado por los estudiantes de la asignatura "Disolventes y métodos de reacción no convencionales" del Máster en Química Sostenible de la Universidad de Zaragoza. No obstante, será bienvenida cualquier contribución que enriquezca el presente wikilibro.
Contenido
| Versión para imprimir |
|---|
- Introducción
- Utilidad de los disolventes
- Impacto económico de los disolventes
- Impacto ambiental de los disolventes
- Clasificaciones de los disolventes según su peligrosidad
- Los disolventes más usados en la Industria Química
- Los disolventes en la Industria Farmacéutica
- La sustitución de los disolventes en la Industria
Desde un punto de vista físico-químico, se denomina disolvente a una sustancia líquida (en las condiciones de aplicación) que disuelve a otras sustancias y puede recuperarse inalterada. Dejando aparte el caso particular del agua, la práctica totalidad de disolventes de interés científico o industrial son compuestos orgánicos. Ateniéndonos ahora a un punto de vista legal, se denomina disolvente orgánico a "todo compuesto orgánico volátil que se utilice solo o en combinación con otros agentes, sin sufrir ningún cambio químico, para disolver materias primas, productos o materiales residuales, o se utilice como agente de limpieza para disolver la suciedad, o como disolvente, o como medio de dispersión, o como modificador de la viscosidad, o como agente tensoactivo, plastificante o protector".[1]
Referencias
- ↑ RD 117/2003 de 31 de enero, BOE de 7 de febrero; Council Directive 1999/13/EC.

Los disolventes son ampliamente utilizados en numerosos procesos tanto a pequeña escala (nivel de laboratorio), como a gran escala (nivel industrial).
La utilidad de los disolventes varía mucho en función de las propiedades que presentan y la cantidad a utilizar en un determinado proceso. Se establece así una clara diferencia entre los distintos usos de los disolventes teniendo en cuenta sus efectos nocivos para la salud humana, de tal forma que muchos de los que se emplean a escala de laboratorio sin presentar ningún tipo de riesgo para los trabajadores, pueden ser altamente peligrosos en caso de ser utilizados a escala industrial. Además, es necesario tener en cuenta que los disolventes se pueden utilizar tanto en forma de disolventes puros como en forma de mezclas de disolventes, destacando que en el último caso, las propiedades de los componentes no se suman sino que la mezcla presenta propiedades nuevas como si se tratase de un disolvente puro.
Evolución de la aplicación de los disolventes en la industria

A lo largo de los años se han utilizado y desarrollado una amplia variedad de disolventes. De forma sencilla, y para generar una idea simple, se presenta a grandes rasgos una breve evolución de los disolventes en la industra [1]
En un inicio, en el ámbito industrial, se comenzaron a utilizar principalmente como disolventes los hidrocarburos derivados del petróleo (hexano o benceno por ejemplo) y los disolventes oxigenados (alcoholes, cetonas, ésteres), a pesar de ser disolventes muy utilizados en la industria tienen asociados ciertos riesgos respecto a la salud humana y al medio ambiente, por lo que en la medida de lo posible se plantea la sustitución de los mismos por otros alternativos. Uno de los tipos de disolventes que se plantean como alternativa son los clorocarbonados , que son bastante seguros en cuanto a su manipulación pero por el contrario son cancerígenos.
A modo de curiosidad, un ejemplo anecdotario sobre como puede surgir la evolución de los disolventes en las industrias, es el uso de CFCs (clorofluorocarbonados) como disolventes, como por ejemplo el CF2Cl--CFCl2 (llamado CFC-113) utilizado en una proporción de 2Kg por metro cuadrado, en la limpieza de grasa, pegamento y residuos de soldadura en paneles de circuito electrónicos tras ser fabricados. Aunque es cierto que principalmente, se empleaban más que como disolventes para la formación de aerosoles y para la creación de refrigerantes . En el caso de utilización de CFCs no se presentaban riesgos por toxicidad en personas pero, sin embargo, resultaron ser perjudiciales para la capa de ozono. Se sustituyeron entonces temporalmente por los HCFCs (hidrógenofluorocarbonados) considerando que esta alternativa era una gran solución, aunque se observó que contribuyen al efecto invernadero de forma que se intenta prescindir de su uso.
Una de las alternativas que se plantea para la sustitución de CFCs y HCFCs es el uso de hidrofluoroéteres esta opción es de gran interés ya que son tan eficaces como CFCs y HCFCs pero presentan la ventaja de no contribuir al efecto invernadero ya que su ODP ( Ozone Depletion Potencial ) es nulo. Los hidrofloroéteres tienen además una ventaja añadida, no son solubles en agua lo que impide la contaminación de la misma.
Con este ejemplo se observa como la necesidad de utilizar disolventes que no sean perjudiciales para el medio ambiente y la salud humana, lleva al desarrollo de nuevos disolventes e incluso al "no uso" en los distintos procesos industriales. Es cierto que es muy difícil conseguir sustituir por completo los disolventes convencionales por otros más verdes en el ámbito industrial ya que no solo supone un reto en cuanto a la investigación de nuevos disolventes, sino también en cuanto a nuevas tecnologías que puedan ser requeridas.
Actualmente la legislación cada vez es más dura en cuanto a la permisibilidad del uso de los disolventes en la industria, por lo que cada vez se planea más el uso de disolventes sostenibles. Esto lleva a las líneas actuales de investigación sobre la sustitución de disolventes convencionales por otros que presenten menos riesgos como es el caso del uso de disolventes neotéricos ( agua, fluidos supercríticos, líquidos iónicos, líquidos fluorosos, polímeros líquidos) en los procesos industriales. Es cierto que el agua fue uno de los primeros disolventes en utilizarse, pero las reacciones en condiciones homogéneas presentan poco interés industrial dada la baja solubilidad de los reactivos y la necesidad añadida de llevar a cabo la extracción de los productos con disolventes orgánicos.
Aplicaciones de los disolventes
Los disolventes industriales son productos líquidos que se pueden emplear como medios de reacción, en procesos de extracción u otras diversas aplicaciones.
Disolventes como medios de reacción
El papel de los disolventes como medio de reacción es muy importante debido a la influencia que ejercen cuando se lleva a cabo una reacción. Un ejemplo de ello es la capacidad que poseen para disolver sustancias, como son los reactivos en estado sólido, de forma que se producen dispersiones homogéneas y como consecuencia un aumento de la reactividad. Además, gracias al poder de disolución que presentan, se facilita el proceso de agitación y mezclado, produciéndose así de forma más eficiente y como consecuencia es una ventaja para los procesos industriales. Una característica importante que presenta el uso de los disolventes como medios de reacción, es la posibilidad de establecer un control del calor, es decir, permiten suavizar las variaciones de temperatura o bien la propia eliminación del calor de una reacción mediante la simple ebullición del mismo. Por ejemplo, en el caso de las reacciones endotérmicas que requieren energía, se le puede suministrar fácilmente calor por calentamiento de la propia disolución. Finalmente, otra de las funciones que puede desempeñar un disolvente como medio de reacción es permitir la precipitación de sólidos. Esta función es importante ya que facilita la separación del sólido ( bien sea el producto o el residuo) de la disolución.
Procesos de extracción
La extracción con disolventes se emplea para la separación de compuestos de interés aprovechando las diferencias de solubilidad de los componentes de la mezcla y el disolvente de extracción adecuado que se haya seleccionado. Con la extracción se permite por tanto obtener el producto de una reacción de forma selectiva o bien eliminar las impurezas que puede contener la mezcla con el producto de interés. Por una parte, este tipo de aplicación presenta una ventaja importante y es que permite que se lleve a cabo la eliminación del disolvente por evaporación, pero sin embargo, tiene como inconveniente que la cantidad de disolvente a emplear es mucho mayor que para el caso de su utilización como medio de reacción. De forma general los procesos de extracción se pueden clasificar como:
• Absorción de gases: este tipo de extracción se produce cuando el material a tratar con el disolvente es un gas, un ejemplo de este tipo de extracción es la eliminación de gases industriales, como el dióxido de carbono, por tratamiento con dietanolaminas.
• Extracción líquido-líquido: este tipo de extracción se produce cuando el material a tratar con el disolvente es un líqido, ejemplo de este tipo de extracción es la eliminación de hidrocarburos aromáticos con furfural en procesos de fabricación de lubricantes.
• Lixiviación: este tipo de extracción se produce cuando el material tratar con el disolvente es un sólido, un ejemplo de este tipo de extracción es la extracción de aceite de semillas oleaginosas.
Otras aplicaciones
Además de utilizarse como medio de reacción o en la extracción de mezclas, los disolventes pueden emplearse en la aplicación y remoción de recubrimientos (pinturas, barnices, lacas), también en el desengrasado de metales, para llevar a cabo la limpieza en seco o en la extracción de productos naturales entre otros usos. Un ejemplo aplicación en el campo de la limpieza es la utilización de los solventes en la limpieza de pinturas y esculturas policromadas en la restauración.[2] En este caso con el disolvente se limpian las manchas y la suciedad superficial, además de eliminar el barniz y repintados.
Algunos disolventes y sus usos
Los disolventes se usan principalmente en el sector industrial de las pinturas, tintas, industria química y farmacéutica, en productos de limpieza, aditivos para la construcción, en la industria del automóvil para llevar a cabo la fabricación de accesorios y en la fabricación de adhesivos. De forma menos importante, ya que la cantidades a utilizar no son tan significativas como en los casos mencionados anteriormente, los disolventes también tienen cabida e importancia histórica por estar presentes en el sector de la metalurgia, en el sector textil, así como en los laboratorios.[3]
Aromáticos
• Tolueno: Es un líquido insoluble en agua con un olor carácterístico al tíner de las pinturas. Se utiliza como disolvente para pinturas, revestimientos, caucho, resinas, diluyente en lacas nitrocelulósicas y en adhesivos.

Anexo: Hoja de seguridad
• Xileno: Es un líquido incoloro derivado del benceno flamable y de olor dulce. Se utiliza como solvente en pinturas, hule, cuero e industria afines.

Anexo: Hoja de seguridad
Acetatos
• Acetato de etilo: Es un líquido volátil y flamable. Se utiliza como disolvente de compuestos utilizados para revestir y decorar objetos de cerámica, para la elaboración de varios compuestos explosivos además de como solvente para la fabricación de películas a base de celulosa en la industria fotográfica.

Anexo: Hoja de seguridad
• Acetato de butilo: Es un líquido incoloro, poco volátil y con un olor a éster frutal y es miscible con todos los disolventes orgánicos comunes. Se emplea como solvente de pinturas, de lacas para la tinción en industria del cuero y como solvente para la elaboración de colorantes.

Anexo: Hoja de seguridad
Cetonas
• Acetona: Es un líquido incoloro, volátil y flamable. Se utiliza como solvente para la mayoría de plásticos y fibras sintéticas,para adelgazar resinas de fibra de vidrio y para limpiar herramientas de fibra de vidrio y disolver resinas de epoxi.

Anexo: Hoja de seguridad
• Metil isobutil cetona (MIBK): Es un líquido incoloro con un olor característico a las bolas de naftalina, se disuelve en agua, alcoholes, bencenos y éteres. Se utiliza como solvente en fabricación de pinturas, hule, químicos y maquinaria.

Anexo: Hoja de seguridad
Alcoholes
• Alcohol metílico o Metanol: Es un líquido incoloro, volátil, venenoso y se disuelve en agua. Se unsa como solvente de tintas, tintes, resinas y adhesivos.

Anexo: Hoja de seguridad
• Alcohol isopropílico o Isopropanol: Es un isómero del propanol incoloro, inflamable, que posee un olor intenso y es miscible en agua. Se usa ampliamente como solvente y como un fluido de limpieza, especialmente para la disolución de aceites.

Anexo: Hoja de seguridad
Clorados
• Percloroetileno (PERC): Es un líquido incoloro, no inflamable, pesado y con un olor similar al éter. Se utilliza como solvente en desengrasado de metales,es un solvente actualmente muy utilizado en las llamadas tintorerías “ecológicas” donde se realizan las denominadas “limpiezas a seco” de tejidos, telas, por su propiedad no inflamable y su alto poder desengrasante. Se emplea en la limpieza de textiles, por su gran poder de limpieza y nula acción sobre las telas y los colores.

Anexo: Hoja de seguridad
• Cloruro de metileno: Es un líquido incoloro, no flamable, volátil y miscible con una amplia variedad de solventes. Se usa como solvente industrial y para eliminar pintura.

Anexo: Hoja de seguridad
Alifáticos
• Gasolvente o Gasnafta: Es un solvente alifático incoloro, con olor a petróleo y se obtiene de los cortes ligeros de nafta. Su principal uso es como adelgazador de pinturas, barnices y extendedor de lacas. También se emplea en tintas para imprenta y textiles, como desengrasador y limpiador de metales.
Anexo: Hoja de seguridad
Glicoéteres
• Butil cellosolve: Es un líquido incoloro que es tanto miscible en agua como en la mayoría de los solventes orgánico. Se usa como solvente en fórmulas de recubrimientos, retardador para lacas, nivelador de película en tintas, para resinas de nitrocelulosa, solvente para aceites minerales.
Anexo: Hoja de seguridad
Mezclas
• Thinner standard: Es un líquido incoloro insoluble en agua. Se emplea como adelgazador de pinturas, para que tenga la consistencia adecuada para ser aplicada con una pistola de aire y como desengrasante de piezas mecánicas.
Anexo: Hoja de seguridad
Disolventes neotéricos
Aunque en la actualidad este tipo de disolventes no tenga una gran aplicación industrial, constituyen un grupo con gran potencial de uso en un futuro.
• Líquidos iónicos: Son sales que funden a bajas temperaturas debido a que su punto de fusión es inferior a 100ºC. Estan formados por iones asimétricos y voluminosos de forma que la fuerzas atractivas son más débiles que en el caso de las sales convencionales. Algunos ejemplos de líquidos iónicos son: el tetrafluoroborato de 1-butil-3-metilimidazolio, el cloruro de 1-butil-3-metilimidazolio y el hexafluorofosfato 1-butil-3-metilimidazolio. Un ejemplo de la aplicación de los líquidos iónicos como disolventes en la industria es el PROCESO DIFASOL, donde se utilizan los líquidos iónicos para efectuar reacciones entre alquenos, el papel que desempeña es el de disolver el catalizador.[4]
• Fluidos supercríticos (FSC): Las aplicaciones más conocidas para este tipo de disolventes están ligadas a procesos de extracción en la industria alimentaria, tabacalera y farmacéutica. Ejemplo de ello es la utilización de FSC para extraer la cafeína del café (1978) o la extracción del lúpulo en la industria cervezera (1982).[5]

Conclusión
Existe una amplia variedad de disolventes que se utilizan en las distintas industrias, desde los convencionales hasta los más novedosos, los neotéricos. Dada la multitud de aplicaciones en las que intervienen, es muy difícil establecer un punto de equilibrio entre los procesos industriales que continúan empleado disolventes convencionales, eficientes pero poco verdes, y nuevos procesos que permitan el uso de disolventes más respetuosos con el medio ambiente, es decir, más sostenibles. Una de las causas posibles es el elevado coste que supondría a las distintas industrias invertir en la adaptación de procesos ya existentes o la implementación de nuevos procesos bien para prescindir de ellos o bien para utilizar disolventes verdes.
Referencias
- ↑ Disolventes industriales - http://www.eii.uva.es/~organica/organica_industrial/material/Tema-13.pdf
- ↑ Los Solventes - http://dglab.cult.gva.es/Archivos/Pdf/DIBAMsolventes.pdf
- ↑ Evaluación y control de la exposición laboral a agentes neurotóxicos. Disolventes industrialesS - http://neurologiadeltrabajo.sen.es/pdf/ponencia2011e.pdf
- ↑ Líquidos iónicos a temperatura ambiente: un nuevo medio para las reacciones químicas - http://www.rac.es/ficheros/doc/00680.pdf
- ↑ Propiedades de los fluidos supercríticos y su utilización como disolventes - http://www.joseluismesarueda.com/documents/TEMA_2.pdf
Bibliografía
- Disolventes y métodos de reacción no convencionales. (Master en Química Sostenible año 2012-2013 de la Universidad de Zaragoza)
- R. Kohli and K. L. Mittal (eds.), Developments in Surface Contamination and Cleaning, 759–871, 2008 William Andrew
- Y. Dai et al. Natural deep eutectic solvents as new potential media for green technology, Analytica Chimica Acta 766 (2013) 61– 68
- E. García Bernal et al. Aplicaciones de los líquidos iónicos en la industria química, Investigación ETSII, Universidad Politécnica de Cartagena
Enlaces externos
- Extracción
- Absorción de gases
- Extracción líquido-líquido
- Lixiviación
- Disolventes verdes
- Disolventes orgánicos
- Solventes industriales
- Tipos de disolventes
- Los diferentes solventes y sus multiples aplicaciones
- Green Solvents Fundamental and Industrial Applications
- líquidos iónicos
- Líquido iónicos y fluidos supercríticos
- Disolventes
- Química delta
- Hojas de seguridad
- Hojas de seguridad
- Hojas de seguridad
Los disolventes son la familia de compuestos químicos más utilizados, ya sea por su capacidad como medio de reacción o agente dispersante, diluyente, tensoactivo, o su uso para limpieza. Esto implica su uso masivo en casi todos los sectores industriales, desde la industria agroalimentaria y de pinturas hasta la industria farmacéutica, y en todos los ámbitos, ya sea en pequeñas y medianas empresas o grandes multinacionales.
Los disolventes industriales más utilizados en la industria son disolventes orgánicos, que se definen como todo “Compuesto Orgánico Volátil” (COVs) que se utilice sólo o en combinación con otros agentes, sin sufrir ningún cambio químico, para disolver materias primas, productos o materiales residuales, o se utilice como agente de limpieza para disolver la suciedad, o como disolvente, o como medio de dispersión, o como modificador de la viscosidad, o como agente tensoactivo, plastificante o protector (Real Decreto 177/2003). Muchos COVs son peligrosos para el medio ambiente y para la salud humana, por ese motivo se han creado restricciones en su uso, como refleja el Protocolo de Montreal, también se presentan alternativas como los disolventes neotéricos, más ecológicos y con características deseables como es el caso de líquidos iónicos, líquidos fluorosos, fluidos supercríticos o en última instancia la química sin disolventes.
Consumo de disolventes en la industria
Los disolventes es una de las familias de productos más utilizada en la industria. Se estima que sólo en la Unión Europea se consumen 2.200.000 toneladas de disolventes. Este genera una importante industria en la que se emplea a más de 10.000 personas en toda Europa. Sus importantes usos hacen que más de medio millón de empresas consuman este tipo de productos, este tipo de empresas tienen unas ganancias de aproximadamente 2.500-3.000 millones de euros y dan empleo a más de 10 millones de personas. Para satisfacer la demanda, la industria de los disolventes gasta más de 20 millones de euros al año y emplea a más de 10.000 personas. [1]. Es decir, ya sea mediante su uso o fabricación la industria de los disolventes es una de las más importantes.
Consumo por países
En el mundo, la región de Asia-Pacífico es la mayor productora de disolventes representando el 39% de la producción mundial. Esto se debeal bajo coste de su transporte y elaboración y a la flexibilidad de legislación. Le sigue Norte América y el Este de Europa [2]. Esta demanda se espera que siga creciendo sobre todo en países emergentes como China, Brasil, India y Rusia debido a la dependencia en estos productos de las diferentes industrias como la de los pesticidas, pinturas y recubrimientos, química, adhesivos, cosméticos, farmacétutica... . Por otra parte, Europa constituye el otro gran mercado de disolventes siendo el mayor consumidor de este tipo de productos, teniendo una cuota de mercado del 26,5% en el mundo. [3]
Consumo por tipo de disolvente
Los disolventes más usados son los alcoholes como el etanol, el n-butanol, isopropoanol y metanol. En el 2011 se usaron 6,4 millones de toneladas de disolventes basados en el alcohol en todo el mundo. Se espera que la demanda para el etanol y éteres aumenten en un 3% entre 2011 y 2019 mientras que los disolventes halogenados decrecen en sus demanda debido principalmente a las restricciones en este tipo de productos en el Oeste de Europa y Norte América. De igual modo, los compuestos hidrocarbonados y aromáticos mantiene esta tendencia decreciente [4].

Uso de disolventes en la industria
La industria que mayor cantidad de disolventes utiliza es la de recubrimientos y pinturas. Sin la presencia de disolventes, las pinturas presentarían una alta viscosidad y sería imposible su aplicación en superficies [5]. El consumo anual de disolventes en esta industria es de 1,5 millones de toneladas. Los disolventes también se emplean en la fabricación de películas fotográficas, son ingredientes de medicamentos y cosméticos,insecticidas, adhesivos y productos de limpieza. Los disolventes también desempeñan un papel importante en la eliminación de pinturas. En el siguiente gráfico se expresan los sectores industriales que más disolventes consumen.
| Proceso industrial | Uso | Tipo de disolvente |
|---|---|---|
| Industria alimentaria | Extracción de aceites y grasa | Ciclohexano y sulfuro de carbono |
| Industria siderúrgica | Limpieza y desengrasado | Tricloroetileno y cloruro de etileno |
| Industria del calzado | Disolvente de colas y pegamentos | Mezcla de hexanos |
| Industria de plástico y caucho | Disolvente de materias primas | Cloroformo y acetona |
| Industria de la madera | Disolvente de lacas y barnices | Tolueno y trementina |
| Industria cosmética | Dispersante | Alcohol etílico, isopropílico y cloroformo |
| Industria de pintura | Diluyente | Tolueno, acetatos y cetonas |
| Limpieza en seco | Disolvente de sustancias orgánicas | Tetracloroetielno |

Hacia disolventes más sostenibles
La preocupación acerca de la emisión de COVs hacia la atmósfera y la creación de nuevos reglamentos que limitan el uso de este tipo de disolvente hace que, sobre todo en la Unión Europea y Norte América, hace que el consumo de disolventes tradicionales se vea sustuido. El ejemplo más notable se encuentra en la industria de las pinturas donde los COVs se han sustituido por pinturas que usan agua o no usan disolventes [6]. Sin embargo, las pinturas basadas en disolventes todavía representan un importante mercado en países en países en vías de desarollo de América Latina, Europa del Este y Asia.
Sustitución de disolventes
Los compuestos oxigenados continúan siendo los más utilizados en la industria mientras que los disolventes verdes, como los líquidos iónicos son los que más rapidámente han crecido en los últimos años [7].

Por otra parte los disolventes halogenados e hidrocarbonados han decrecido en los últimos años en los países desarollados debido a las fuertes restricciones o prohibiciones de estos productos, intentándolos sustituir por disolventes más sostenibles.
El problema reside en el alto coste y la accesibilidad a los nuevos disolventes, por ejemplo el coste de los líquidos iónicos ronda entre los 2800-6000€/kg, para los líquidos flurosos los 20-500€/kg [8] mientras que el de un disolvente convencional como el tolueno no supera los 30€ [9].
Conclusiones
La industria de los disolventes es un mercado que mueve millones en todo el mundo, ya sea en su fabricación en los mercados emergentes ya sea debido a la demanda masiva en países desarollados, al estar presentes en la mayoría de procesos de fabricación industrial. Sin embargo, debido a las nuevas legislaciones y restricciones de uso de algunos compuestos orgánicos, la sustitución de estos productos por alternativas más verdes deberá de ser un hecho en los próximos años. Las alternativas, como los líquidos iónicos, son más caras debido a su costosa fabricación o debido a la necesidad de adaptar los procesos de producción, pero a largo plazo los beneficios mediambientales compensarán la inversión.
Referencias
- ↑ http://www.esig.org/en/about-solvents/what-are-solvents/facts-and-figures-the-european-solvents-industry-in-brief
- ↑ http://www.ceresana.com/en/market-studies/chemicals/solvents/
- ↑ http://www.prweb.com/releases/oxygenated_solvents/green_solvents/prweb4677774.htm
- ↑ http://www.ceresana.com/en/market-studies/chemicals/solvents/solvents-market-share-capacity-demand-supply-forecast-innovation-application-growth-production-size-industry.html
- ↑ http://www.sigmaaldrich.com/analytical-chromatography/air-monitoring/applications/paints-and-coatings/solvents.html
- ↑ http://www.pcimag.com/articles/96310-global-solvents-market-to-reach--33-billion
- ↑ http://www.prweb.com/releases/oxygenated_solvents/green_solvents/prweb4677774.htm
- ↑ http://www.synquestlabs.com/
- ↑ http://www.sigmaaldrich.com/chemistry/solvents.html
Bibliografía
- Disolventes y métodos de reacción no convencionales. Máster en Química Sostenible 2012-2013, Universidad de Zaragoza
- Fundamentos de Sostenibilidad. Máster en Química Sostenible 2012-2013, Universidad de Zaragoza
- Cinet Magazine.Number 1. September 2006
- Paul T. Anastas; John C. Warner, Green Chemistry: Theory and Practice,1998, Oxford University Press.
Debido a las prácticas industriales, la utilización de los disolventes ha generado una buena modificación de la reactividad, disolución de sustancias, eficaz transporte de masa y energía, entre otros. Pero que a su vez presentan riesgos para la salud de los seres vivos y la preservación del medio ambiente, ya que el problema con los disolventes no es tanto su empleo como lo mal asociado con su contención, recuperación y reutilización.
En la actualidad, han aumentado las consideraciones ambientales ocupando un lugar cada vez más importante en la industria química, saciando el deseo de los consumidores preocupados y los fabricantes para elegir los productos más respetuosos para el medio ambiente; este ha llevado al desarrollo de la evaluación del ciclo de vida (LCA) y el diseño para el medio ambiente (DfE). Evitando o eliminando grandes cantidades de emisiones provenientes del uso desmedido de los disolventes en la industria.
Peligros para la salud
Todos los beneficios que mejoran la calidad de vida, resultan innegables las diversas formas de contaminación y los incidentes graves en forma de explosión, incendios, intoxicaciones masivas, pueden ser causa de incidentes personales o públicos altamente dramáticos que tienen con gran frecuencia origen en el uso de los disolventes en la actividad química industrial.
El carácter volátil de los disolventes hace que éstos se evaporen rápidamente en el aire, alcanzando concentraciones importantes en espacios confinados. Los riesgos mayores para el ser humano se producen por la absorción de éstos a través de la piel y por inhalación. El contacto directo con la piel permite que el disolvente pase a la sangre, causando efectos inmediatos y a más largo plazo. La inhalación constituye la vía de exposición más peligrosa, porque los pulmones son muy eficaces en distribuir éstas, o cualquier otra sustancia, por todo el cuerpo pudiéndose inhalar concentraciones muy elevadas en plazo breve, siendo esta vía, además, particularmente difícil de controlar. [1]
Los efectos sobre la salud pueden variar según el compuesto, estos dependerán de la naturaleza de cada compuesto y del grado y del periodo de exposición al mismo. Según el 10º Informe sobre Carcinógenos, se sabe que el benceno es un carcinógeno humano y se presume razonablemente que el formaldehído y el percloroetileno son carcinógenos. Las personas con mayor riesgo de exposición a largo plazo a esos tres compuestos orgánicos volátiles son los trabajadores industriales que tienen una exposición ocupacional prolongada a los compuestos, los fumadores y las personas expuestas por períodos prolongados a las emisiones del tránsito pesado de vehículos automotores.
Exposición e Intoxicación
El mayor campo de contacto, es en las industrias donde el trabajador expuesto al disolvente, como consecuencia de esa exposición, puede desarrollar un daño en su organismo. Ese daño será proporcional a una serie de factores como son:
- Los propios de la naturaleza humana.
- Los característicos de los disolventes (su toxicidad).
- La velocidad de absorción por el organismo.
- La concentración en el ambiente.
- Tiempo de exposición.
Para que un trabajador se vea afectado por un tóxico,no dependerá sólo de la dosis recibida, sino también de la forma y el tiempo que tarde en administrarse esa dosis. Hay 3 tipos de intoxicaciones según su velocidad de penetración en el organismo: aguda, subaguda y crónica. [2]
Prevención
Son aquellas medidas cuyo objeto es impedir que los riesgos a los que está expuesta la trabajador den lugar a situaciones de emergencia.
Las acciones de prevención las aplicamos:
- Foco contaminante.
- Medios de propagación.
- El individuo.
Foco contaminante
Sustituir un disolvente por uno de menor toxicidad. Ejemplo: el tricloroetileno por el 1,1,1 tricloroetano
Medios de propagación
Generar una ventilación localizada, realizar la limpieza por procedimientos húmedos o aspirado (equipos que pierden disolventes, en contacto con la atmósfera, se evaporan y se mezclan con el aire) y sistemas de alarmas para el aumento desproporcional de concentraciones en el foco contaminante.
Individuo
Sobre el individuo puede actuarse en su buen uso de la higiene y protección personal, la formación e información sobre el disolvente a tratar en el trabajo diario. Como también hacer rotaciones, para disminuir la exposición del trabajador.
Alternativas
Existen sistemas de limpieza de piezas que eliminarían la necesidad de utilizar disolventes, y que ofrecen mejores resultados que los procesos tradicionales:
- Limpieza acuosa automatizada.
- Lavado acuoso con potencia.
- Limpieza ultrasónica.
- Flujos bajos en sólidos.
- Soldadura en atmósfera inerte.
Existen otras experiencias prácticas, que demuestran la existencia de numerosas tecnologías que son más respetuosas con la salud de trabajadores/as y el medio ambiente y la viabilidad económica de las mismas. Un ejemplo es el caso de una empresa mediana en EE.UU, fabricante de herramientas, que sustituyó su sistema de desengrase de las piezas basado en tricloetileno por un agente no tóxico y biodegradable, el d‐limoneno, que es una sustancia química natural que se extrae a partir de la esencia de cítricos principalmente.
Ademas de calcular:
- Valores umbral límites (TLV): concentración a la que la mayoría de los trabajadores puede exponerse sin riesgos durante un período de 8 horas.
- Concentraciones máximas autorizadas (CMA): para los venenos aerotransportados. [3]
Peligros para el medio ambiente
Los productos químicos causantes de la contaminación del ambiente son también nocivos y peligrosos, pero a través de efectos que se manifiestan de manera no inmediata y que ademas permanecen durante periodos prolongados de tiempo.
La industria química suele emplear sustancia químicas en cantidades elevadas, con riesgo de vertidos ocasionales o de emisiones mejor o peor controladas. En la siguiente tabla, se muestra los datos de sustancias toxicas emitidas por la Industia quimica de Estados Unidos, según datos de la Environmental Protection Agency de Estados Unidos (EPA). [4]
| Producto | Emisiones | Producto | Emisiones |
|---|---|---|---|
| Ácido clorhídrico | 657 | Ácido clorhídrico | 65 |
| Hidróxido sódico | 627 | n-Hexano | 72 |
| Metanol | 420 | Metanol | 241 |
| Tolueno | 345 | Tolueno | 127 |
| Acetona | 235 | Metiletilacetona | 60 |
| 1,1,1-Tricloroetano | 182 | Ácido fosforico | 63 |
| Diclorometano | 152 | Diclorometano | 54 |
| TOTAL | 2618 | TOTAL | 682 |
Los efectos nocivos de los productos emitidos al ambiente dependen naturalmente de su toxicidad, pero también de su persistencia y su movilidad en el ambiente. La vida media de los disolventes en medioambiente es alta.
Compuestos Orgánicos Volátiles (COV)
El uso de disolventes orgánicos suponen el 30%, del que aproximadamente el 20% representa el uso de disolventes en la industria. La evaporación de los disolventes orgánicos a partir de su uso en la industria, como ya se ha dicho, contribuye en una parte muy importante a estas emisiones. Basta indicar que entre los sectores de producción y aplicación de pinturas, el de impresión y las actividades de desengrase y limpieza de metales se produce el 65% de las emisiones.
Las emisiones de COV representan millones de toneladas anuales (directivas 99/13/CE, programa CAFÉ, REACH). [5]
Provocando consecuencia a su exposición:
A CORTO PLAZO
- Irritación ocular.
- Molestias nasales y de garganta.
- Jaquecas.
- Reacciones cutáneas alérgicas.
- Disnea.
- Naúseas.
- Fatiga.
- Mareo.
A LARGO PLAZO
- Lesiones del hígado.
- Los riñones.
- El sistema nervioso central. [6]

La emisión de compuestos orgánicos volátiles (COVs) a la atmósfera tiene algunos problemas importantes para el medio ambiente. Algunos COVs contribuyen a la degradación de la capa de ozono atmosférico, como es el caso del 1,1,1‐tricloroetano y el tetracloruro de carbono, así como de los CFCs y los HCFCs, entre otros.
Por otro lado, los COVs junto con los NOx en presencia de luz solar actúan como precursores de la formación de ozono troposférico y smog fotoquímico (Limitación de niveles, Directiva 92/72/CEE). Causando efectos nocivos para las especies vegetales y los cultivos, interfiriendo en las actividades fotosintéticas, en el crecimiento y en el metabolismo general, aumentando la sensibilidad de los árboles a las heladas, al calor y a la sequía.
Smog Fotoquímico
Contribuyen a la formación del smog fotoquímico al reaccionar con otros contaminantes atmosféricos (como óxidos de nitrógeno y con la luz solar, formando oxidantes fotoquímicos troposféricos (como formaldehído, monóxido de carbono e hidroperoximetilo. Este smog fotoquímico se da principalmente en áreas urbanas, dando lugar a atmósferas ricas en ozono de un color marrón.
La formación y destrucción de ozono:
Durante el día el dióxido de nitrógeno se disocia en monóxido de nitrógeno y radicales oxígeno:

:NO2 + hν → NO + O·
El O se combina con oxígeno molecular generando ozono:
:O· + O2 → O3
En ausencia de COVs este ozono oxida al monóxido de nitrógeno de la etapa anterior:
:O3 + NO → O2 + NO2
Pero en presencia de COVs, éstos se transforman en radicales peroxi que a su vez oxidan al NO:
:ROO· + NO → RO· + NO2
De esta forma el NO no está disponible para reaccionar con el ozono y el OZONO se acumula en la atmósfera. Muchos de los radicales RO· generados terminan formando aldehídos. Éstos, cuando la concentración de NO es baja (conforme avanza el día), pueden reaccionar con NO2 dando lugar a compuestos del tipo RCOOONO2 (cuando R es un metilo se denomina peróxido de acetilnitrato, PAN, un compuesto tóxico).
La formación del HNO3 se produce al final del día por reacción del NO2 con radicales oxhidrilo:

Durante la noche los radicales OH· pueden reaccionar con el NO dando ácido nitroso, que se disocia en presencia de luz, pero es estable durante la noche.
OH· + NO → HONO
HONO + hν → OH· + NO
Durante la noche las reacciones de smog fotoquímico se ven muy reducidas al necesitar la luz para funcionar, aunque éstas pueden continuar a través de otros compuestos. [7]
Legislación aplicable
La Unión Europea ha aprobado la Directiva sobre los COVs "Directiva del Consejo relativa a la limitación de las emisiones de compuestos orgánicos volátiles debidas al uso de disolventes orgánicos en determinadas actividades e instalaciones". El objeto de esta Directiva es prevenir y minimizar los efectos directos e indirectos de las emisiones de compuestos orgánicos volátiles al medio ambiente, principalmente a la atmósfera, y los riesgos potenciales para la Salud Humana, por medio de medidas y procedimientos que deben implementarse en las actividades definidas en su Anexo I.
- Directiva 96/61/CE relativa a la prevención y al control integrados de la contaminación (IPPC) que establece un sistema de autorizaciones para actividades industriales tomando en cuenta determinadas sustancias contaminantes sobre las que fijará valores límite de emisión para concesión del correspondiente permiso. Uno de los compuestos a tener en cuenta es el de los órgano volátiles o metales y sus compuestos. En octubre de 1999 se deberá transponer en el Estado español.
- Directiva 76/769 relativa a la aproximación de las disposiciones legales reglamentarias y administrativas de los estados miembros que limitan la comercialización y el uso de determinadas sustancias y preparados peligrosos.
- Directiva 67/548 relativa a la aproximación de las disposiciones legales, reglamentarias y administrativas en materia de clasificación, embalaje y etiquetado de las sustancias peligrosas.
- Directiva 92/72/CEE sobre la contaminación atmosférica por ozono troposférico.
- Real Decreto 1494 de setiembre de 1995 que desarrolla la anterior directiva en España.
- Ley de prevención de relaciones laborales sobre manipulación de sustancias peligrosas.
- Ley 10/1998 sobre residuos.
- Real Decreto 833/1998 por que se modifica lo relativo al Reglamento sobre residuos tóxicos y peligrosos.
- Ley 11/1997 de Envases y Residuos de Envases, de 24 de abril.
- Real Decreto 149/1989 sobre clasificación, envasado y etiquetado de pinturas y productos afines.
- Real Decreto 150/1989 sobre clasificación , envasado y etiquetado de disolventes.
- Real Decreto 74/1992 por que se aprueba el reglamento nacional de transporte de mercancías peligrosas por carretera.
- Real Decreto 2216/1985 Reglamento sobre declaración de sustancias nuevas y clasificación, envasado y etiquetado de sustancias peligrosas.[8]
Verdor
En la utilización de disolventes no solo se evalúa la toxicidad, sino también se establecen propiedades de su verdor, como es:
- Energía de evaporación, presurización, agitación entre otros.
- Reciclado.
- Solubilidad del soluto.
- Toxicidad atómica del proceso.
- Separación de los productos.
- Posible influencia en el producto/empaquetado.
Conclusión
Es importante para las industrias contar con formas adecuadas que permitan la comparación cuantitativa entre dos o más procesos o productos en los que se refiere a su impacto ambiental. Aparte de las cuestiones de balance económico y de sensibilidad social, la evaluación de la cantidad de residuos que genera y de su peligrosidad, es decir, de su capacidad nociva, requiere disponer de parámetros para la diversas formas de toxicidad, y eco-toxicidad, influencia en el calentamiento global, la capa de ozono estratosférico, la generación de ozono troposférico, riesgo de inflamación, etc.
Valorando la sustitución de los disolventes orgánicos clásicos por otros de origen renovable, que superen los riesgos y la contaminación.
Referencias
Bibliografía
- R. Mestres, Química Sostenible, Editorial Síntesis,(2011). 105–143.
- Disolventes y métodos de reacción no convencionales. ( Máster en Química Sostenible año 2012-2013 de la Universidad de Zaragoza)
- Wj. Crinnion, et al. (2010): The CDC fourth national report on human exposure to environmental chemicals: what it tells us about our toxic burden and how it assist environmental medicine physicians. Altern Med Rev,15(2):101-9.
- P.H. Howard, et al, Handbook of Environmental Degradation Rates, Lewis, 1991.
- M.C Mancheño, et al, Exposición Laboral a Disolventes, Unión Sindical de Madrid Región de CCOO, 2008.
Enlaces internos
Enlaces externos
- Emisiones procedentes de la industria
- Exposición humana a químicos ambientales
- Compuestos orgánicos volátiles
- EPA
- Troposfera y legislaciones
- Disolventes
Los disolventes son muy comunes en muchos lugares de trabajo en los que los trabajadores se olvidan de lo peligrosos que pueden resultar. Se entiende por disolvente aquella sustancia, habitualmente líquida, que se utiliza para disolver otra sustancia. Aunque estos pueden utilizarse en ocasiones sin riesgo alguno, pueden provocar problemas de salud al contacto con la piel o al inhalar sus vapores. Otros de los riesgos son los vapores de muchos disolventes, que son inflamables y explosivos, e incluso muchos son dañinos para el medio ambiente.
Parámetros de peligrosidad en disolventes
Para determinar si un disolvente utilizado en la industria es peligroso, para la salud humana y medio ambiente, se han establecido unos parámetros que nos dan información acerca del peligro del uso de estas sustancias.
Los parámetros más importantes a la hora de etiquetar un producto químico según su peligrosidad son:
Punto de inflamación (Flash Point)
El punto de inflamación se corresponde con el Flash Point, que es la temperatura mínima necesaria para que un material inflamable desprenda vapores que, mezclados con el aire, se inflamen en presencia de una fuente ígnea, para volverse a extinguir rápidamente por sí sola una vez retirada la fuente de activación.
Este parámetro es mayor en sustancias con puntos de ebullición (Te) altos. Por ejemplo, se puede estimar de forma orientativa para hidrocarburos a partir del punto de ebullición (Te) mediante la siguiente fórmula[1]:
- ti = 0,683 Te -71,7
- ti = 0,683 Te -71,7
Respecto a la peligrosidad, no interesa que este parámetro sea bajo, ya que conlleva a una alta inflamabilidad.
| Disolvente | Flash Point (ºC) |
|---|---|
| Pentano | - 40 |
| Hexadecano | 126 |
| Decano | 46 |
| Benceno | -11 |
| Clorobenceno | 30 |
| Bromobenceno | 51 |
| Diclorometano | - |
| Triclorometano | - |
| Agua | - |
Temperatura de autoignición
Se denomina temperatura de autoignición a la temperatura mínima de un sustancia a la que puede arder en ausencia de una fuente de ignición, normalmente mediante contacto con una superficie caliente como lineas de vapor, tuberías de aceite, etcétera. A esta temperatura se alcanza la energía de activación suficiente para que se inicie la reacción de combustión.
Este parámetro recibe también el nombre de temperatura o punto de autoencendido, temperatura de ignición espontánea o autógena y hasta puede aparecer solamente como temperatura de ignición.
| Disolvente | Tª de autoignición (ºC) |
|---|---|
| Disulfuro de carbono | 90 |
| Eter dietílico | 160 |
| Acetaldehido | 175 |
| Heptano | 204 |
| Hexano | 225 |
| Alcohol etílico | 365 |
| Metanol | 385 |
| Acetona | 465 |
| Benceno | 560 |
| Diclorometano | 615 |
En general, los alcanos y los éteres presentan bajas temperaturas de autoignición, mientras que los compuestos halogenados presentan valores altos.
Límites de explosión
También llamados límites de explosividad, existen dos términos principales:
- Límite inferior de explosividad: Corresponde a la concentración de vapor en el “flash point”,es decir, el punto de inflamacion a la que la ignición conduce a una explosión.
- Límite superior de explosividad: Concentración de vapor que es demasiado rica para explotar, es decir, la máxima concentración del gas en el aire por encima de la cual una explosión no es posible.
Estos parámetros dependen de la concentración de oxígeno, concentración de gases distintos al oxígeno, tipo de gas inerte y concentración, tamaño del equipo, dirección de propagación y presión, temperatura y composición de la mezcla.
| Productos | Inferior | Superior |
|---|---|---|
| Hidrógeno | 4.1 | 74.2 |
| Metano | 5.3 | 13.9 |
| Acetileno | 2.5 | 80.0 |
| Etileno | 3.02 | 34.0 |
| Etano | 3.12 | 15.0 |
| Propano | 2.37 | 9.5 |
| n-butano | 1.6 | 8.5 |
| Pentano | 1.4 | 8.0 |
| Hexano | 1.25 | 6.9 |
| Ciclohexano | 1.31 | 8.35 |
| Benceno | 1.40 | 8.0 |
| Dietiléter | 1.9 | 36 |
Límites de explosividad (% Volumen en aire) Los éteres y alcoholes presentan amplios intervalos de explosión.
Formación de peróxidos
Los peróxidos son sustancias que presentan un enlace oxígeno-oxígeno y que contienen el oxígeno en estado de oxidación = −1. Por lo tanto, se comportarán habitualmente como sustancias oxidantes. En contacto con material combustible pueden provocar incendios o incluso explosiones.
Respecto a la formación de estos a partir de disolventes en la industria, un ejemplo son los éteres, que tienen grupos CH unidos al oxígeno que pueden formar hidroperóxidos. La reacción requiere oxígeno y se acelera por luz, catalizadores metálicos y aldehídos. En contacto con material combustible pueden provocar incendios o incluso explosiones, y por ello son tan peligrosos.
Los éteres se suelen almacenar sobre KOH, ya que destruye los peróxidos y actúa como desecante. Los éteres no suelen usarse a escala industrial por esta tendencia a explotar.
Daño inmediato y norma de exposición ocupacional
- Daño inmediato para la vida y la salud: Máxima concentración de vapor de la que una persona puede escapar en 30 minutos sin daño irreversible para su salud o sin efectos que le impidan escapar.
- Norma de exposición ocupacional: Exposición a un disolvente en el aire a las que no hay indicación de daños causados incluso tras exposiciones diarias en jornadas de 8 horas.
Toxicidad de los disolventes
La toxicidad es un término general que se refiere a cualquier efecto adverso o daño que es resultado de la exposición a una sustancia química o a cualquier otra sustancia. Puede considerarse como una propiedad molecular inherente e inalterable que depende de la estructura química, aunque también depende, en gran medida, del organismo con el que la sustancia entre en contacto.
Dentro de la familia de los disolventes se pueden establecer unas categorías según las características de toxicidad:
- Carcinógeno: Aquel que actúa sobre los tejidos vivos de tal forma que produce cáncer.
- Mutágeno: Agente físico, químico o biológico que altera o cambia la información genética (usualmente ADN) de un organismo y ello incrementa la frecuencia de mutaciones por encima del nivel natural.
Clasificaciones de peligrosidad
NFPA 704 (National Fire Protection Agency)
NFPA 704 es el código que explica el "diamante de materiales peligrosos" establecido por la Asociación Nacional de Protección contra el Fuego, utilizado para comunicar los riesgos de los materiales peligrosos. El rombo NFPA 704 nos permite identificar los riesgos asociados a los materiales peligrosos; fue diseñado para identificar materiales en almacenamientos, sin embargo, es también usado para contenedores durante el transporte.
Los aspectos más importantes en esta norma son los colores y números que se asignan para indicar el nivel de riesgo.
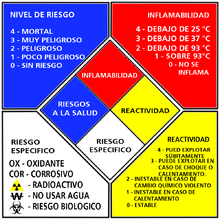
Las cuatro divisiones tienen colores asociados con un significado:
- Azul: Peligros para la salud.
- Rojo: Amenaza de inflamabilidad.
- Amarillo: Peligro por reactividad.
- Blanco: Indicaciones especiales para algunos materiales, indicando que son oxidantes, corrosivos, reactivos con agua o radiactivos.
Las divisiones azul, roja o amarilla tienen valores de 0 (sin peligro) a 4 (peligro máximo).
Glaxo - Smith - Kline
GlaxoSmithKline (GSK) es una empresa británica de productos farmacéuticos, productos de cuidado dental y de cuidado de la salud. Esta empresa es el resultado de la fusión de Glaxo Wellcome y SmithKline Beecham. A su vez, es una empresa de investigación bioquímica y sus productos abarcan una gran parte en el campo de la farmacia.
Esta empresa realizó una guía[2] sobre los diferentes disolventes que se utilizan en la industria química, clasificándolos según una serie de parámetros característicos de estas sustancias, entre los que se encuentran los descritos anteriormente al inicio del capítulo. Inicialmente, estaba formada por 47 sustancias, sin embargo, debido a las nuevas investigaciones y mayores conocimientos se ha incrementado el número hasta 110.
Se marcan los diferentes parámetros de peligrosidad asociados a cada disolvente y a un color en particular, estos colores indican la peligrosidad del disolvente conforme al parámetro indicado:<b
- Amarillo:Sustitución recomendada - No existen restricciones actualmente, pero en el futuro se deberían aplicar.
- Naranja: Sustitución recomendada - Se aplican restricciones de regulación.
- Rojo: Tiene que ser sustituido - Se aplica la prohibición.
Se puede observar que los disolventes más peligrosos según esta clasificación son:
- Triclorometano
- Cloroformo
- Dicloroetano
- 2- Metoxietanol
- Benceno
Estudiando los dos tipos de clasificaciones se puede observar que el gran trabajo realizado por GlaxoSmithKline nos deja una clasificación realmente amplia y muy detallada sobre una gran cantidad de disolventes, su riesgo y parámetros de peligrosidad, e incluso su impacto sobre el medio ambiente. La clasificación NFPA 704 se podría decir que es más sencilla, ya que contiene información más general con un número de parámetros menor, y a la vez más práctica en la mayor parte de las industrias.
Además de las clasificaciones explicadas anteriormente existen otras clasificaciones; por ejemplo, el Método EHS (Environmental Health and Safety) y el Método LCA (Life Cycle Assessment)
Referencias
- ↑ NTP 379: Productos inflamables: variación de los parámetros de peligrosidad. Instituto Nacional de Seguridad y Salud en el Trabajo http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/NTP/Ficheros/301a400/ntp_379.pdf
- ↑ GSK Solvent Selection Guide 2009 http://www.rsc.org/suppdata/gc/c0/c0gc00918k/c0gc00918k.pdf
Bibliografía
- Disolventes y métodos de reacción no convencionales. (Máster en Química Sostenible, año 2012-2013, Universidad de Zaragoza)
- " Handbook of Solvents". G. Wypych, Chemtech, 2001
- "Solvents and solvent effects in organic chemistry", C. Reichardt.
- "The properties of Solvents", Y. Marcus, Wiley, Volume 4", Universidad de Jerusalem, Israel.
- " Solvent - free organic synthesis", T. Koichi
Enlaces externos
- Environmental Health and Safety
- Life Cycle Assessment
- Secretaria de Energía - República de Argentina
- Fichas de Seguridad
Los disolventes son usados en la industria química, en una gran variedad de procesos, como medios de reacción, ya que disuelven sustancias, producen dispersiones homogéneas (con el soluto repartido de manera equitativa por toda la mezcla) aumentando la reactividad, mejoran el mezclado y la agitación, mejoran el control del calor en el proceso y permite el precipitado de sólidos. También son utilizados como extractantes (extracción o separación de compuestos), para desengrasado, limpieza de máquinas, etc. La utilización de unos disolventes u otros para cada proceso, dependerá de las características propias de los mismos. Éstos parámetros nos definen cada disolvente desde un punto de vista de seguridad (puntos de inflamación, autoignición, etc) y de su adecuación o no para cada uso (viscosidad, densidad, polaridad, etc).
REFERENCIAS
Bibliografía
- F. Hortal Sánchez: "Métodos de la industria química 2." Editorial Reverté S.A., p.92 (1987)
- Hans Beyer, Wolfgang Walter: "Manual de química orgánica." Editorial Reverté S.A. (1988)
Introducción
Los hidrocarburos son compuestos formados por carbono e hidrógeno. Se clasifican en hidrocarburos alifáticos y aromáticos. Pueden ser moléculas cíclicas o de cadena abierta, ramificada o lineal, saturada o insaturada, siendo su nomenclatura la siguiente:
- alcanos y cicloalcanos —hidrocarburos saturados
- alquenos —hidrocarburos insaturados con uno o más dobles enlaces
- alquinos—hidrocarburos insaturados con uno o más triples enlaces
Las fórmulas generales son CnH2n+2 para los alcanos, CnH2n para los cicloalcanos, CnH2n para los alquenos, y CnH2n-2 para los alquinos.

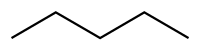




El estado de los hidrocarburos alifáticos a temperatura ambiente depende del número de carbonos que poseen y de su estructura. Los hidrocarburos que tienen desde uno a cuatro carbonos son gaseosos (por ejemplo: metano, etano o etileno). Los hidrocarburos con más de cinco carbonos son líquidos, por ejemplo, el hexano o el octano. Y los hidrocarburos con más diecisiete carbonos son sólidos. Este es el caso del heptadecano.
Los hidrocarburos alifáticos de uso industrial derivan principalmente del petróleo, que es una mezcla compleja de hidrocarburos. Se obtienen por craqueo, destilación y fraccionamiento del petróleo crudo. Los más utilizados como disolventes son: pentano, hexano, heptano, ciclohexano y metilciclohexano. Los alquenos y alquinos se utilizan como productos de partida en síntesis química.
Propiedades físico-químicas
| Pentano | Hexano | Heptano | Ciclohexano | Metilciclohexano | |
|---|---|---|---|---|---|
| CAS | 109-66-0 | 110-54-3 | 142-82-5 | 110-82-7 | 108-87-2 |
| Color/forma | Líquido incoloro | Líquido incoloro | Líquido incoloro | Líquido incoloro | Líquido incoloro |
| Peso Molecular (g/mol) | 72,1 | 86,2 | 100,2 | 84,2 | 98,2 |
| Punto de ebullición (°C) | 36 | 69 | 98 | 81 | 101 |
| Punto de fusión (°C) | -129 | -95 | -90 | 7 | -126,7 |
| Densidad relativa (agua = 1) | 0,63 | 0,7 | 0,68 | 0,8 | 0,8 |
| Solubilidad en agua | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna |
| Presión de vapor (kPa a 20°C) | 56,8 | 17 | 4,8 | 12,7 | 5,73 |
| Densidad relativa de vapor (aire = 1) | 2,5 | 3,0 | 3,46 | 2,9 | 3,4 |
| Punto de inflamación (°C) | -49 | -22 | -1 | -18 | -6 |
| Temperatura de autoignición (°C) | 309 | 225 | 215 | 260 | 258 |
| Límites de explosividad(% en volumen en el aire) | 1,5-7,8 | 1,1-7,5 | 1,1-6,7 | 1,3-8,8 | 1,2-6,7 |
| Coeficiente de reparto octanol/agua (log Pow) | 3,39 | 3,90 | 4,66 | 3,40 | 3,61 |
Peligrosidad
Todos estos hidrocarburos son altamente inflamables y las mezclas vapor/aire son explosivas.
Como medidas de prevención se deben de evitar las llamas, no producir chispas y no fumar. El pentano no debe estar en contacto con oxidantes fuertes y el ciclohexano con superficies calientes.
La clasificación de estos disolventes según la NFPA 704 aparece recogida en la siguiente tabla.[1]

| Hidrocarburo | Riesgo a la salud | Inflamabilidad | Reactividad | Riesgo especial |
|---|---|---|---|---|
| Pentano | 3 | 4 | 0 | - |
| Hexano | 3 | 3 | 0 | - |
| Heptano | 3 | 3 | 0 | - |
| Ciclohexano | 3 | 3 | 0 | - |
| Metilciclohexano | 3 | 3 | 0 | - |
La mayoría de los incendios causados por hidrocarburos líquidos se deben a un escape de los mismos llegado a una fuente de ignición o extendiéndose y evaporándose rápidamente. Un ejemplo sería la explosión que tuvo lugar en 1974 en Flixborough (Reino Unido). Este accidente de debió a un escape unas 40 Tm de ciclohexano que formó una nube inflamable e inmediatamente se produjo una explosión de vapor no confinada al entrar en contacto con una fuente de ignición. [2] [3]
Efectos tóxicos
Los hidrocarburos alifáticos superiores al etano son depresores del sistema nervioso central. Los vapores producen una ligera irritación de las mucosas. Se puede decir que en general, la toxicidad de los alcanos aumenta al hacerlo el número de carbonos de la molécula. Los hidrocarburos saturados líquidos son disolventes de grasas e irritantes de la piel. El contacto repetido o prolongado con la piel, la seca y desengrasa, con resultado de irritación y dermatitis. El contacto directo de los hidrocarburos líquidos con el tejido pulmonar a través de la inhalación produce neumonitis química, edema pulmonar y hemorragia. La intoxicación crónica por hexano o mezclas que contengan hexano puede causar polineruopatía.
El hexano puede entrar en el organismo vía inhalación o a través de la piel siendo su absorción lenta. El hexano tiende a evaporarse cuando se ingiere produciéndose su rápida dilución en el aire alveolar y un descenso del oxígeno, con asfixia y lesión cerebral o parada cardíaca. El hexano tiene una toxicidad aguda tres veces superior que el pentano. Los efectos crónicos se producen por exposición prolongada a dosis que no producen síntomas agudos aparentes. Después de que aparezcan los primeros síntomas se produce el agravamiento de la deficiencia motora de las regiones afectadas en un principio y su extensión a otras. La lesión suele extenderse de los miembros inferiores a los superiores. En casos graves de intoxicación se han observado síntomas en el sistema nervioso central (defectos de la función visual o de la memoria). En la ruta metabólica del hexano, éste se transforma en 2-hexanol que a su vez se transforma en 2,5-hexanodiol y 2,5-hexanodiona. Éste último metabolito es el más tóxico.
Los cicloalcanos producir efectos tóxicos por inhalación e ingestión, tienen una acción irritante y desengrasante de la piel. Son anestésicos y depresores del sistema nervioso central.
La toxicidad aguda del ciclohexano es muy pequeña. Los vapores de ciclohexano causan un leve y corto efecto anestésico, pero más potente que el del hexano. Los experimentos con animales han demostrado que el ciclohexano es mucho menos nocivo que el benceno. El metilciclohexano tiene efectos tóxicos similares pero menos intensos que el ciclohexano.
Uso en la industria
El uso de disolventes derivados de los hidrocarburos del petróleo en Europa es inferior al 10%. En España la situación es similar.[4]
Los hidrocarburos saturados se usan como combustibles, lubricantes y disolventes. También se pueden utilizar como materias primas para la síntesis de plásticos, detergentes, pesticidas o productos químicos.
El pentano es uno de los agentes espumantes primarios que se usan en la producción de espuma de poliestireno. El heptano se usa como combustible para motores o como disolvente. El hexano se usa principalmente como disolvente de gomas, colas en muebles y bolsos de cuero, cementos y adhesivos para el calzado. Se puede usar como adhesivo para papeles de pared, en la fabricación de impermeables, en el recauchutado de neumáticos y en la extracción de aceites vegetales. El hexano se utiliza también como agente limpiador en las industrias de tejidos, muebles y cuero. La mayoría del ciclohexano producido se transforma en la mezcla ciclohexanona-ciclohexanol que se utiliza para la obtención de ácido adípico y caprolactama que se utilizan para la síntesis del nylon. Sin emabrgo, el ciclohexano junto con el hexano forma la mezcla conocida como "hexano comercial" que se utiliza como disolvente en la industria del calzado.
Impacto ambiental
Los compuestos orgánicos volátiles, a veces llamados VOC (siglas en inglés), o COV (siglas en español), se convierten fácilmente en vapores o gases. Este término agrupa a una gran cantidad de compuestos químicos, entre los que se incluyen los hidrocarburos alifáticos. El uso de los hidrocarburos alifáticos como disolventes en la industria hace que se liberan a la atmósfera, principalmente hexano.

La liberación de COVs al aire se puede comparar con su capacidad para formar ozono en relación a etileno (factor de producción de ozono troposférico o POCP). En 2003, el POCP relacionado con emisiones de disolventes fue de 2,21 millones de kilogramos equivalentes a etileno. Los alquenos tienen un factor POCP igual a 84 y los alcanos, 42. Estos valores indican que los alcanos y especialmente los alquenos pueden formar ozono. Cuando estos compuestos se mezclan con óxidos de nitrógeno, reaccionan para formar ozono y producir el conocido smog fotoquímico.
En la siguiente gráfica se recogen las emisiones de hidrocarburos (COV) que se produjeron en 2009 en los países de la Unión Europea.[5]

Sustitución por disolventes alternativos
Debido a la toxicidad del hexano éste se puede sustituir por disolventes menos tóxicos como el ciclohexano, el heptano y el metilciclohexano ya que sus propiedades físicas y químicas son similares.
Además de sustituir hexano por estos disolventes, existen otras alternativas que se están estudiando en las empresas para eliminar el uso de estos disolventes.[6] Algunos ejemplos son los siguientes. En la extracción de aceites vegetales se puede utilizar dióxido de carbono en lugar de hexano. En la industria del calzado se pueden unir los adornos mediante adhesivos al agua o cinta adhesiva a dos caras en lugar de utilizar heptano. En el tapizado de muebles se puede sustituir el hexano por adhesivos al agua o grapas. En la industria papelera se utiliza hexano para pegar papel pero se podría emplear cinta adhesiva.
REFERENCIAS
- ↑ http://www.newenv.com/resources/nfpa_chemicals/
- ↑ http://www.aiche.org/ccps/topics/elements-process-safety/commitment-process-safety/process-safety-culture/flixborough-case-history
- ↑ http://www.unizar.es/guiar/1/Accident/Flix.htm
- ↑ http://www.magrama.gob.es/es/calidad-y-evaluacion-ambiental/temas/sistema-espanol-de-inventario-sei-/06_Uso_de_Disolventes_y_Otros_Productos_-_VNC_tcm7-219786.pdf
- ↑ http://www.esig.org/publications/194/40/esig-esvoc-coordination-group-solvent-voc-emissions-inventories-position-paper/?cntnt01currentpage=1&cntnt01limit=5&cntnt01detailpage=publications&cntnt01orderby=Date+DESC&cntnt01template=display_home_list&cntnt01origid=15
- ↑ http://www.istas.net/fittema/att/di8.htm
Bibliografía
- V. Aguirre Yela: "Obtención de pentanos, hexanos, heptanos y octanos a partir de las fracciones de los derivados livianos del petróleo." Escuela politécnica del ejército. Vol 14 (2011)
- Fichas Internacionales de Seguridad Química
- Monografía XII. Contaminación y Salud. Capítulo IX: Compuestos orgánicos volátiles en el medio ambiente. José María Sánchez Montero y Andrés R. Alcántara León. 2007. Monografías de la Real Academia Nacional de Farmacia
Introducción
Los hidrocarburos son compuestos formados únicamente por átomos de hidrógeno y carbono, pudiéndose considerar los esqueletos a partir de los cuales y por inserción de grupos funcionales se generan formalmente todas moléculas orgánicas. En el caso de los hidrocarburos arómaticos, también conocidos por el nombre genérico de arenos (bencenos sustituidos), se trata de compuestos que presentan al menos un ciclo con dobles enlaces conjugados (alternación de enlace sencillo y doble) y con un total de 4n+2 electrones pi en el anillo, es decir, que cumplen la regla de Hückel.El ejemplo más básico y representativo de esta familia de compuestos es el benceno, sustancia con fórmula C6H6 que presenta una estructura de ciclo plano hexagonal donde los carbonos ocupan los vértices y cada uno de ellos está ligado a un hidrógeno. En esta molécula los carbonos están unidos por enlaces sencillo y doble alternadamente, pero si se realizan medidas de las longitudes de enlace se observa que todos ellos presentan una longitud intermedia entre un enlace sencillo C-C y uno doble. Esto es debido a que los 6 electrones pi presentes en el anillo están deslocalizados en la molécula (no se mantienen en un determinado enlace), este fenómeno al que se denomina aromaticidad otorga estabilidad a la molécula al permitir la existencia de varias formas resonantes.
Aunque es el fenómeno de aromaticidad el punto en común de los hidrocarburos aromáticos, el adjetivo que los caracteriza es previo al descubrimiento de su peculiar estructura electrónica y les fue asignado porque muchos de los compuestos de esta familia poseen un fuerte aroma, si bien en ocasiones no es especialmente agradable como sucede en el caso del benceno. Dentro de los hidrocarburos aromáticos se pueden definir dos subfamilias de compuestos: los hidrocarburos aromáticos monocíclicos (del inglés MAH) si poseen un único anillo de benceno y los policíclicos (PAH) cuando poseen varios. A su vez, dentro de estos últimos se encuentran los policíclicos condensados cuando los anillos comparten al menos dos carbonos con el ciclo vecino (naftaleno). Algunos ejemplos:
- Algunos arenos
-
Benceno
-
Tolueno
-
Cumeno
-
p-Xileno
-
m-Xileno
-
Anilina
-
Nitrobenceno
-
Ácido Benzoico
-
Paracetamol
-
Naftaleno (PAH)
Producción
Las fuentes principales de obtención de estos compuestos son la hulla (mediante destilación) y el petróleo (mediante diversos procesos petroquímicos: destilación, alquilación). También se pueden obtener de algunas plantas como los pinos, las aromáticas o eucaliptos cuyos aceites esenciales contienen terpenos y p-cimeno. En el caso de los PAH, además de poder obtenerse controladamente con fines comerciales, se forman involuntariamente en la combustión incompleta de materia orgánica[1] (quema de carbón, gas, madera, basura, tabaco, carne asada al carbón) suponiendo un problema medioambiental y para la salud dado los efectos adversos que al menos parte de ellos han mostrado.
Propiedades Físico-químicas
Las propiedades de reactividad química vienen marcadas por la aromaticidad del anillo que hace a estas moléculas muy estables termodinámica y cinéticamente. El benceno y el resto de arenos, no dan fácilmente las reacciones típicas de adición de los sistemas insaturados (hidrogenación, hidratación, halogenación u oxidación). De hecho muchos de ellos pueden usarse como disolvente gracias a su baja actividad. En la tabla se recogen las propiedades de algunos compuestos representativos de esta familia.
| Benceno[2] | Cumeno[3] | Naftaleno[4] | Tolueno[5] | |
|---|---|---|---|---|
| Apariencia | Líquido transparente incoloro | Líquido incoloro | Sólido blanco cristalino | Líquido incoloro |
| Punto de ebullición (°C) | 80 | 152.4 | 217.9 | 111 |
| Punto de fusión (°C) | 5.5 | -96.0 | 80.2 | -95 |
| Peso Molecular(g/mol) | 78.11 | 120.19 | 128.16 | 92.13 |
| Solubilidad en agua | ligeramente soluble | insoluble | insoluble | insoluble |
| Densidad relativa (agua = 1) | 0.8765 | 0.862 | 1.0253 | 0.87 |
| Densidad de vapor relativa (aire = 1) | 2.7 | 4.2 | 4.42 | 3.1 |
| Presión de vapor (kPa a 20°C) | 10 | 10 mmHg a 38.3°C | 0.01 | 3.8 |
| Punto de inflamación (°C) | -11 | - | 80 | 4 |
| Temperatura de autoignición (°C) | 500 | - | 540 | 480 |
| Límites de explosividad (% en volumen en el aire) | 1.2-8.0 | 0.9-6.5 | 0.9-5.9 | 1.1-7.1 |
| Coeficiente de reparto octanol/agua (log Pow) | 2.13 | 3.66 | 3.3 | 2.69 |
Peligrosidad
La National Fire Prevention Association (NFPA) clasifica a la mayoría de los hidrocarburos aromáticos con un código de inflamabilidad de 3 (donde 4 significa riesgo grave). Por ello, al presentan un riesgo de ignición considerable siempre que se trabaje con ellos se debe evitar la acumulación de sus vapores y recoger inmediatamente las fugas y derrames, además de evitar la proximidad de fuentes de calor extremo. Como se puede observar en la tabla anterior para la mayoría de los hidrocarburos aromáticos los vapores son bastante más densos que el aire por lo que se extienden a ras del suelo y se puede dar la ignición en un punto distante a la fuente de la que procede la sustancia. Con el fin de evitar riesgos mayores, hay que tener en cuenta a la hora de elegir el material de trabajo que algunos de estos compuestos son buenos disolventes para plásticos y caucho (como el benceno o el tolueno).
Efectos tóxicos
La entrada al organismo de los hidrocarburos aromáticos puede darse por inhalación, ingestión y en menor cantidad por vía cutánea. Una vez dentro del organismo, éste trata de degradarlos a compuestos hidrosolubles que se conjugan con glicina, ácido glucurónico o sulfúrico para poder ser excretados por la orina, la principal ruta de eliminación de estos compuestos. En general, los bencenos con un sustituyente son más tóxicos que los que tienen dos sustituyentes alquilo, y en los que la cadena es ramificada aun es mayor la toxicidad. Esto es debido a que en el organismo se metabolizan a compuestos hidrosolubles por oxidación del anillo, pero cuando el anillo tiene sustituyentes alquílicos se oxidan estos en lugar del anillo.
Es una familia muy amplia y variada de compuestos por lo que la toxicidad varía mucho dentro de ella, aquí sólo se recogen algunos efectos tóxicos que pueden causar. Los más comunes para intoxicación aguda (dosis puntual) son la irritación de las vías respiratorias produciendo tos y dolor de garganta, también genera dolor de cabeza, náuseas, mareo, palpitaciones, desorientación, confusión e inquietud. En caso de dosis altas se puede dar incluso la pérdida de conocimiento y depresión respiratoria, pudiendo llegar a causar la muerte. En cuanto a los efectos por exposición crónica (dosis continuadas en un periodo largo de tiempo), los síntomas neurológicos pueden ser: cambios de conducta, depresión, alteraciones del estado de ánimo y cambios de personalidad y de la función intelectual y neuropatía distal. Otros efectos crónicos son sequedad, irritación y agrietamiento de la piel y dermatitis.
Hay evidencias de que varios hidrocarburos aromáticos como el benceno (cancerigeno de clase 1 según la DFG)[6] o algunos PAH son cancerígenos[7].
[8]
Para evitar los efectos nocivos para la salud debidos a la inhalación de estos compuestos en el lugar de trabajo es muy importante evitar su presencia en el aire, por lo que hay que trabajar con extracción localizada, mantener los recipientes bien cerrados cuando no se usen y adoptar las precauciones necesarias para evitar fugas o derrames. Además de estas medidas comunes, los trabajadores en contacto con estos productos tendrán que emplear equipos de protección individual (EPI´s) como mascaras, guantes, ropa de protección adecuada, etc. según indique el manual de Prevención de Riesgos Laborales.
Uso en la industria
Los principales usos de los hidrocarburos aromáticos puros son: síntesis química de plásticos (estireno), caucho sintético, pinturas, pigmentos (anilina), explosivos, alimentación (benzaldehido = condimento artificial, ácido benzoico = conservante), pesticidas (naftaleno = control de polillas y parasitos del ganado, y reactivo de partida para síntesis de insecticidas), detergentes, perfumes (anisol) y fármacos (fenol = antiséptico, acetofenona = droga hipnótica). También se usan como mezclas como disolventes y como constituyentes, en proporción variable, de la gasolina.
Algunos ejemplos de compuestos empleados como disolvente:
- Benceno: se ha empleado como disolvente en formulaciones y para extracciones de sustancias partiendo de semillas y frutos secos. También se ha usado en la fabricación de estireno, fenoles, anhídrido maleico, detergentes, explosivos, productos farmaceúticos y colorantes, y como combustible. Actualmente está prohibido su uso en las formulaciones de productos para uso doméstico y en muchos países también está prohibido su uso como disolvente y componente de los disolventes para limpieza en seco.
- Cumeno: es un buen disolvente de grasas y resinas, lo que ha llevado a usarlo en la industria como sustituyente del benceno. Se emplea como disolvente de pinturas y lacas de celulosa, como componente de alto octanaje para combustibles de aviones y como materia prima (obtención de fenol y acetona, obtención de estireno por pirolisis).
- Tolueno: disolvente de aceites, resinas, caucho, alquitrán de hulla, asfalto, brea y acetilcelulosas. Se emplea como disolvente y diluyente en pinturas, barnices de celulosa en tintas de fotograbado. Mezclado con agua forma una mezcla azeotrópica con efecto deslustrante. Se emplea en la formulación de productos de limpieza para determinadas industrias y artesanía.
Impacto ambiental

Varios hidrocarburos aromáticos, como el benceno, tolueno o xileno, están dentro de los denominados COVs (Compuestos Orgánicos Volátiles[9][10]), uno de los principales grupos de sustancias responsables de la contaminación atmosférica ya que además de los efectos nocivos que generan per se también participan en la formación de ozono troposferico. Debido a los daños para la salud y medioambiente se ha ido estableciendo legislación para controlar las emisiones de estos COVs, en España tenemos el RD 117/2003[11] (que transpone la directiva 1999/13) que limita la emisión de COVs debido al uso de disolventes o el RD 227/2006 (transposición de Directiva 2004/42/CE[12]) que regula la emisión de COVs en determinadas pinturas, barnices y productos de renovación del acabado de vehículos.
La mayoría de estos compuestos son dañinos para los medios acuáticos y algunos, como el cumeno, para el ambiente en general (Ver referencias 2 a 5).
Sustitución por otros disolventes
En la industria se viene buscando la sustitución de sustancias tóxicas por otras que sean menos dañinos para la salud y el medio ambiente, siempre que haya una sustancia igual de eficaz y menos dañina debería tratar de llevarse a cabo la sustitución ya que es el método de prevención más eficaz[13].
[14]
En el caso del benceno si bien no es fácil sustituirlo cuando se emplea como reactivo en síntesis química si que se han ido encontrando sustitutos para la mayoría de sus usos como disolvente. El disolvente alternativo a veces no es tan buen pero el ahorro económico u otra propiedad, puede compensar su menor capacidad como disolvente. Algunos sustitutos son derivados del benceno como el tolueno o xileno, otros disolventes son el ciclohexano, hidrocarburos alifáticos (puros o mezclas), naftas, derivados del petróleo…Además, según la función del material que se quiera disolver y de que proceso industrial se trate también se pueden usar cetonas, alcoholes, esteres y derivados clorados del etileno.
Para el tolueno, cuando se emplea en los adhesivos para la industria de cuero o del mueble se puede sustituir por adhesivos al agua o empeando fusión por calor o sujección mecánica (grapas), en su uso en imprentas se puede sustituir también por agua (a presión o caliente para limpieza)y en desengrasado de materiales se puede sustituir por una disolución acuosa básica.
Referencias
- ↑ Agencia para Sustancias Tóxicas y el Registro de Enfermedades http://www.atsdr.cdc.gov/es/phs/es_phs69.html
- ↑ Ficha Internacional de Seguridad Química del Benceno http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/0a100/nspn0015.pdf
- ↑ Ficha Internacional de Seguridad Química del Cumeno http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/101a200/nspn0170.pdf
- ↑ Ficha Internacional de Seguridad Química del Naftaleno http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/601a700/nspn0667.pdf
- ↑ Ficha Internacional de Seguridad Química del Tolueno http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/0a100/nspn0078.pdf
- ↑ Web de la DFG http://www.dfg.de/en/service/press/press_releases/2004/index.html
- ↑ http://www.murciasalud.es/pagina.php?id=252725&idsec=1573
- ↑ ATSDR http://www.atsdr.cdc.gov/es/phs/es_phs69.html
- ↑ http://www.istas.ccoo.es/ecoinformas/index.asp?idpagina=621
- ↑ http://www.juntadeandalucia.es/medioambiente/site/portalweb/menuitem.7e1cf46ddf59bb227a9ebe205510e1ca/?vgnextoid=22fe6d15fad28310VgnVCM1000001325e50aRCRD&vgnextchannel=36e08c43b07d4310VgnVCM1000001325e50aRCRD
- ↑ RD 117/2003 http://www.boe.es/buscar/doc.php?id=BOE-A-2003-2515
- ↑ Directiva 2004/42/CE http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CELEX:32004L0042:ES:HTML&lr=lang_es
- ↑ Guía de CCOO para delegad@s de prevención sobre "Sustitución de Sustancias Disolventes Peligrosas" http://www.istas.ccoo.es/descargas/guia%20disolventes.pdf
- ↑ http://www.istas.net/fittema/att/dif.htm
Bibliografía
- K. Peter, C. Vollhardt y N. E. Schore."Química Orgánica". Ediciones Omega (1996).
- J.L. Soto Cámara. "Química Orgánica. I. Conceptos básicos". Editorial Síntesis (1996).
- Enciclopedia de la OIT (Organización internacional del trabajo). Vol. IV. Capítulo 104.6 (2001).
Tolueno

El tolueno tiene una fórmula molecular de C7H8 . Se obtiene del petróleo crudo y en el árbol tolú. También se produce durante la manufactura de gasolina y de otros combustibles a partir de petróleo crudo y en la manufactura de coque a partir de carbón. Químicamente se genera en la ciclodehidrogenación del n-heptano y además se obtiene como subproducto en la generación de etileno y de propeno. Algunas de sus características principales son:
- Punto de ebullición: 383,8K (111ºC)
- Viscosidad: 0,590 cP
- Solubilidad en agua: 0,47g/L H2O
El tolueno se adiciona a los combustibles (como antidetonante) y como disolvente para pinturas, revestimientos, caucho, resinas, diluyente en lacas nitrocelulósicas y en adhesivos. Es el producto de partida en la síntesis del TNT (2,4,6-trinitrotolueno), un conocido explosivo. De igual modo, el tolueno es un disolvente ampliamente utilizado en síntesis,también se puede utilizar en la fabricacion de colorante.
En cuanto a la peligrosidad, su punto de inflamación está en 277K (4ºC), y su temperatura de autoignición en 873K (600ºC), por lo que es altamente inflamable, pero se necesita una alta temperatura para que arda espontáneamente. Se trata de un disolvente nocivo, puede afectar al sistema nervioso. Es biodegradable pero tóxico para la vida acuática.
Introducción
Los haloalcanos son un conjunto de compuestos químicos derivados de los alcanos, en el que uno o varios hidrógenos han sido sustituidos por átomos de halogeno. En función del tamaño de la cadena podemos encontrar halometanos, haloetanos, haloalcanos de cadena larga y polímeros. Otra clasificación posible es en función del átomo de halógeno que sustituye al hidrógeno: fluoroalcanos, cloroalcanos, bromoalcanos y yodoalcanos. También son posibles compuestos mixtos, siendo los más conocidos los clorofluorocarbonos (CFC) que son los principales responsables del agujero de ozono. Los haloalcanos han sido ampliamente utilizados en la industria, pero debido a la toxicidad y al daño que ejercen al medioambiente, muchos de ellos han sido sustituidos por otro tipo de disolventes.
Propiedades
En lineas generales los haloalcanos se parecen a sus alcanos correspondientes en que son incoloros, prácticamente inodoros e hidrofóbicos. Sus puntos de ebullición son mayores y se incrementa a medida que el peso molecular del compuesto aumenta. Esto es debido a una mayor fortaleza de las interacciones intermoleculares tipo London y dipolo-dipolo. Los haloalcanos, en general, al contener menos enlaces C-H son menos inflamables que sus alcanos correspondientes. Son bastante más reactivos que sus análogos sin átomos de halógeno.
Diclorometano
El diclorometano (DCM) o cloruro de metileno, es un compuesto orgánico con fórmula CH2Cl2. Es un líquido volátil, incoloro, con un leve aroma dulce que es utilizado en la industria como disolvente.
Propiedades físico-químicas
* Apariencia: Líquido incoloro * Solubilidad en agua: 1.3 g/100 mL (20ºC) * Densidad: 1.33 g/cm3 * Presión de vapor: 47.4 kPa (20°C) * Masa molar: 84.933 g/mol * Coeficiente reparto octanol agua: 1.25 * Punto de fusión: -95ºc (177,9 K) * Límites de explosividad, % v en aire: 12-25 * Punto de ebullición: 40ºc (313 K) * Densidad relativa de vapor (aire = 1): 2.9


Producción
El DCM es producido de forma industrial mediante una reacción entre el metano o cloro metano y cloro gas a unas condiciones de temperaturas de 400-500ºC.
CH4 + Cl2 →CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
Usos industriales
Gracias a su volatilidad y su capacidad de disolver una amplia gama de compuestos orgánicos, el diclorometano es utilizado como disolvente en una gran variedad de productos químicos. Es utilizado como agente desengrasante y para eliminar pinturas. Su volatilidad se utiliza como un agente de soplado para espumas de poliuretano . También puede encontrarse en algunos aerosoles y pesticidas. En la industria alimentaria , se ha utilizado durante mucho tiempo para extraer la cafeína del café y del té, así como para preparar extractos de lúpulo y otros aromas, pero debido a su toxicidad, ha sido reemplazado por otros disolventes más verdes y sostenibles como el CO2 supercrítico.
Toxicidad
El diclorometano se puede absorber por inhalación y por ingestión. Por evaporación de esta sustancia a 20°C se puede alcanzar muy rápidamente una concentración nociva en el aire. En el organismo es metabolizado a monóxido de carbono lo que puede llevar a envenenamiento por esta sustancia. Los efectos de corta duración pueden afectar a la piel, los ojos y el tracto respiratorio, causando vómitos, neumonías, irritación ocular, formación de carboxihemoglobina y una disminución del estado de alerta. en cuanto a la exposición prolongada o repetida, puede causar dermatitis por contacto con la piel, afectar al sistema nervioso central e hígado. Además es considerada un sustancia carcinógena en humanos. Tiene un olor medianamente agradable, y cuando se inhala, se siente un frescor en la garganta lo cual ofrece una sensación de placer entre la población joven.
Peligrosidad
En contacto con superficies calientes o con llamas esta sustancia se descompone formando humos tóxicos y corrosivos. Reacciona violentamente con metales como polvo de aluminio y de magnesio, bases fuertes y oxidantes fuertes, originando peligro de incendio y explosión. Ataca algunas formas de plásticos, caucho y revestimientos.
Cloroformo
El cloroformo o triclorometano, es un compuesto orgánico con fórmula CHCl3. Es un líquido incoloro volátil, de olor característico.
Propiedades físico-químicas
* Apariencia: Líquido incoloro * Solubilidad en agua: 0.8 g/100 mL (20ºC)) * Densidad: 1.483 g/cm3 * Presión de vapor: 21.0861 kPa (20°C) * Masa molar: 119.38 g/mol * Coeficiente reparto octanol agua: 1.97 * Punto de fusión: -63.5ºC (209.7 K) * Densidad relativa de vapor (aire = 1): 4.12 * Punto de ebullición: 61.2ºC (334.3 K)
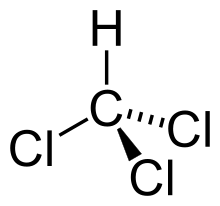

Producción
El cloroformo es producido en grandes cantidades de forma natural, especialmente a través de algas marinas. Industrialmente, se produce mediante una reacción entre el metano o cloro metano y cloro gas a unas condiciones de temperaturas de 400-500ºC.
CH4 + Cl2 →CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
Usos industriales
Como disolvente es bastante común, ya que es miscible con gran cantidad de compuestos orgánicos. Es muy utilizado en la industria farmacéutica y para la producción de colorantes y pesticidas. Es un disolvente muy efectivo para alcaloides, empleándose en la extracción de la morfina, procedente de la amapola, y de la escopolamina, procedente de plantas del género Datura. El cloroformo deuterado, CDCl3 se utiliza como disolvente en espectroscopia RMN.
Como reactivo, uno de sus usos principales es la producción de clorodifluorometano, precursor para la obtención de tetrafluoroetileno, que es empleado en la producción de teflón.
CHCl3 + 2 HF → CHClF2 + 2 HCl
Toxicidad
El cloroformo se puede absorber por inhalación,a través de la piel y por ingestión. Efectos de exposición de corta duración: irritación ocular, daños en el hígado, riñón y sistema nervioso central (antiguamente se utilizaba como anestésico), puede causar náuseas, dolor de cabeza y pérdida del conocimiento. Sus efectos pueden aparecer de forma no inmediata, y se recomienda vigilancia médica. En cuanto a los efectos de exposición prolongada: efectos adversos en el hígado y en el riñón, al ser una sustancia desengrasante, puede causar daños en las membranas lipídicas de los órganos. Es una sustancia considerada como posible carcinógena en seres humanos.
Peligrosidad
En presencia de oxígeno y en contacto con superficies calientes o llamas, el cloroformo puede descomponerse formando humos tóxicos, como HCl, fosgeno o vapores de cloro. Reacciona violentamente con bases fuertes, oxidantes fuertes, algunos metales, como aluminio, magnesio y zinc, originando peligro de incendio y explosión.
Tetracloruro de carbono
El tetracloruro de carbono es un compuesto inorgánico con fórmula CCl4, es un líquido incoloro con un cierto olor dulce. En la década de los 80 fue muy utilizado como extintor de incendios, agente de limpieza y precursor de CFC's ampliamente empleados en esa época como refrigerantes con fines industriales. Desde los años 90, a raíz del descubrimiento del agotamiento de la capa de ozono mediante la acción de los CFC's y su prohibición tanto en su producción como en su comercialización a través del Protocolo de Montreal, la producción de CCl4 descendió bruscamente.
Propiedades físico-químicas
* Apariencia: Líquido incoloro * Solubilidad en agua: 0.1 g/100 mL (20ºC)) * Densidad: 1.5867 g/cm3 * Presión de vapor: 12.2 kPa (20°C) * Masa molar: 153.82 g/mol * Coeficiente reparto octanol agua: 2.64 * Punto de fusión: −22.92°C (250.23 K) * Densidad relativa de vapor (aire = 1): 5.3 * Punto de ebullición: 76.72°C (349.87 K)


Producción
En la década de los 50, se preparaba por cloración de sulfuro de carbono a 105-130 ºC.
CS2 + 3 Cl2 → CCl4 + S2Cl2
Hoy en día la principal reacción para producir CCl4 es a partir de la reacción entre metano y cloro.
CH4 + 4 Cl2 → CCl4 + 4 HCl
También se pueden obtener a partir de diclorometano, cloroformo u otros clorocarbonos de orden mayor.
C2Cl6 + Cl2 → 2 CCl4
Usos industriales
Durante la segunda mitad del siglo 20, este compuesto, fue ampliamente utilizado en la industria. Sus principales aplicaciones eran como refrigerante y como extintor de incendios, debido a su escasa inflamabilidad. A su vez se utilizó como precursor de otros compuesto utilizados como refrigerantes y agentes de extinción de incendios: CFC's, que debido a su capacidad de agotamientro del ozono fue prohibido su uso y comercialización. Como disolvente se utiliza en la investigación de síntesis química, pero debido a sus efectos tóxicos se trata de remplazarlo por otros disolventes menos nocivos, como el tetracloroetileno.
Puede servir como un disolvente para espectroscopia infrarroja , ya que no hay bandas de absorción significativas mayores de 1600 cm -1 . Debido a que no tiene ningún átomo de hidrógeno, se utilizado históricamente en H-RMN.
El CCl4 es un hepatotóxico muy potente, y se utiliza en la investigación de agentes hepatoprotectores.
Toxicidad
Se puede absorber por inhalación,a través de la piel y por ingestión. La sustancia puede causar efectos en hígado, riñón y sistema nervioso central, dando lugar a pérdida del conocimiento, puede darse estado de coma e incluso la muerte. Puede producir irritación ocular. El contacto prolongado o repetido con la piel puede producir dermatitis. Esta sustancia es posiblemente carcinógena para los seres humanos.
Peligrosidad
El CCl4 no tiene prácticamente inflamabilidad a temperaturas bajas. En contacto con superficies calientes o con llamas esta sustancia se descompone formando humos tóxicos y corrosivos, tales como el fosgeno. En cuanto al medioambiente, es un agotador de la capa de ozono y un gas de efecto invernadero, pero a raíz del Protocolo de Montreal su concentración en la atmósfera ha disminuido.
1,2-dicloroetano
También conocido como dicloruro de etileno, es un hidrocarburo clorado, que a temperatura ambiente se presenta en estado líquido, incoloro y de olor parecido al cloroformo. Históricamente, se ha utilizado como pesticida para fumigar plantas y terrenos. Debido a su alta volatilidad y persistencia en el aire, puede liberal radicales cloro, que intervengan en las reacciones de destrucción de ozono. Su potencial agotador de ozono es bajo y por ello no se incluyo en el Protocolo de Montreal, pero actualmente su uso y comercialización para algunas aplicaciones esta prohibido. Actualmente se utiliza para producir cloruro de vinilo.
Propiedades físico-químicas
* Apariencia: Líquido incoloro * Solubilidad en agua: 0.87 g/100 mL (20ºC) * Densidad: 1.253 g/cm3 * Presión de vapor: 8.7 kPa (20°C) * Masa molar: 98.96 g/mol * Coeficiente reparto octanol agua: 1.48 * Punto de fusión: -35ºC (238 K) * Límites de explosividad, % v en aire: 6.2-16 * Punto de ebullición: 84ºC (357 K) * Densidad relativa de vapor (aire = 1): 3.42


Producción
Se produce en grandes cantidades (aproximadamente 20 millones de toneladas anuales). Su principal ruta de síntesis es a partir de la reacción entre etileno y cloro gas, catalizada por cloruro de hierro (III).
H2C=CH2 + Cl2 → ClCH2-CH2Cl
Otra vía para la síntesis de este compuesto es mediante una reacción de oxicloración de etileno catalizada con cloruro de cobre (II).
H2C=CH2 + 4 HCl + O2 → 2 ClCH2-CH2Cl + 2 H2O
Usos industriales
El principal uso del 1,2-dicloroetano es la producción de cloruro de vinilo, precursor del polímero policloruro de vinilo (PVC).
Cl-CH2-CH2-Cl → H2C=CH-Cl + HCl
El 1,2-dicloroetano es un buen disolvente aprótico polar, que se podría utilizar como desengrasante y removedor de pintura, pero en la actualidad está prohibido el uso debido a su toxicidad y carcinogenicidad.
Toxicidad
Por evaporación, esta sustancia a 20º C se puede alcanzar muy rápidamente una concentración nociva en el aire, provocando dolores abdominales, tos, vértigo, somnolencia, dolor de cabeza y garganta, náuseas, vómitos y pérdida del conocimiento. Según estudios epidemiológicos, existen evidencias claras de que el 1,2-dicloroetano es un posible cancerígeno para los seres humanos. Una exposición repetida a este compuesto puede provocar alteraciones funcionales en el sistema nervioso central, riñón e hígado. Por contacto con la piel y los ojos provoca enrojecimiento y sensibilización, y si la exposición es prolongada puede causar dermatitis.
Peligrosidad
Con respecto a su incidencia en el medio ambiente, se trata de una sustancia extremadamente inflamable, que se descompone al calentarla intensamente y al arder, produciendo humos tóxicos y corrosivos similares a los producidos por el cloroformo(ácido clorhídrico y fosgeno) que se liberan a la atmósfera. Debido a su gran persistencia y lenta degradación, puede permanecer muchos años en el medio ambiente, provocando alteraciones severas en la fauna y flora autóctona. A su vez al ser precursor de radicales cloro, puede considerarse como una sustancia con potencial agotador de ozono.
Referencias
- https://en.wikipedia.org/wiki/Haloalkane
- http://repository.lasallista.edu.co/dspace/bitstream/10567/1037/1/Extraccion_cafeina_Coffea_arabica_fluidos_super_criticos.pdf
- http://www.semarnat.gob.mx/archivosanteriores/temas/gestionambiental/calidaddelaire/Documents/20%20preguntas%20de%20Ozono.pdf
- http://www.norden.org/en/publications/publikationer/2003-516/at_download/publicationfile
- http://ozone.unep.org/new_site/sp/montreal_protocol.php
- Deficiencia de vitamina A potencia inducida por tetracloruro de carbono-fibrosis hepática en ratas
Enlaces externos
- [9]Ficha de seguridad diclorometano INSHT
- [10]Ficha de seguridad cloroformo INSHT
- [11]Ficha de seguridad 1,2-dicloroetano INSHT
- [12]Ficha de seguridad tetracloruro de carbono INSHT
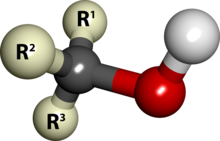

Introducción
Los alcoholes son compuestos orgánicos que contienen un grupo hidroxilo (-OH), que se encuentra unido a una cadena hidrocarbonada a través de un enlace covalente a un átomo de carbono con hibridación sp3, además este carbono debe estar saturado, es decir, debe tener solo enlaces simples a sendos átomos; esto diferencia a los alcoholes de los fenoles.

Una clase importante de alcoholes son los alcoholes acíclicos simples , la fórmula general es CnH2n+1OH . De éstos, etanol (C2H5OH) es el alcohol que se encuentra en las bebidas alcohólicas ; en el lenguaje común la palabra alcohol se refiere a etanol.
Según la IUPAC el sufijo "ol" aparecerá en el nombre de todas las sustancias en las que el grupo hidroxilo sea el grupo funcional con la prioridad más alta; en sustancias donde esté presente un grupo de mayor prioridad se utilizará el prefijo "hidroxi". El sufijo "ol" en nombres no sistemáticos (como el paracetamol o el colesterol) también indica normalmente que la sustancia incluye un grupo funcional hidroxilo. Sin embargo, muchas sustancias, en particular azúcares (ejemplos de glucosa y sacarosa) contienen grupos funcionales hidroxilo sin utilizar el sufijo.
Metanol

El metanol, también conocido como alcohol metílico, alcohol de madera, nafta de madera o espíritu de madera, es un producto químico con fórmula CH3OH (a menudo abreviado MeOH). El metanol adquirió el nombre de "alcohol de madera", ya que se obtenía principalmente como un subproducto de la destilación destructiva de la madera. El metanol se trata de un alcohol que se sintetiza mediante un proceso catalítico a partir de monóxido de carbono e hidrógeno. Esta reacción emplea altas temperaturas y presiones, y necesita reactores industriales grandes y complicados.«Obtención de metanol». Algunas de sus características principales son:
- Punto de ebullición: 337,8K (65ºC)
- Viscosidad: 0,59 mPa•s (20ºC)
- Solubilidad en agua: totalmente miscible
Es un disolvente industrial y se emplea como materia prima en la fabricación de formaldehído. También se emplea como anticongelante en vehículos, combustible, solvente de tintas, tintes, resinas, adhesivos, biocombustibles y aspartamo. El metanol puede ser también añadido al etanol para hacer que éste no sea apto para el consumo humano y para vehículos de modelismo con motores de combustion interna.
En cuanto a la peligrosidad, su punto de inflamación está en 285K (12ºC), y su temperatura de autoignición en 658K (385ºC), por lo que es inflamable a temperaturas no muy elevadas, pero se necesita una alta temperatura para que arda espontáneamente.
La acción tóxica del metanol viene dada por su oxidación metabólica en ácido fórmico o formaldehído. El metanol tiene una alta toxicidad en los seres humanos. La ingesta de tan solo 10 ml de metanol puro puede causar ceguera permanente por la destrucción del nervio óptico, y 30 mL son potencialmente mortales, aunque la dosis letal media es típicamente 100 ml, es decir, 1-2 ml/kg de peso corporal de metanol puro. Dosis de referencia para el metanol es de 0,5 mg/kg/día.
Etanol

El etanol, también llamado alcohol etílico o alcohol puro, es un líquido volátil, inflamable, incoloro, con fórmula CH3CH2OH estructural, a menudo abreviado como C2H5OH o C2H6O. El etanol es una droga psicoactiva y es una de las drogas recreativas más antiguas todavía vigentes en los seres humanos. El etanol puede causar intoxicación por alcohol cuando se consume. Mejor conocido como el tipo de alcohol que se encuentra en las bebidas alcohólicas, que también se utiliza en los termómetros, como disolvente, y como combustible. El tiene una fórmula molecular de C2H6O. Se trata de un alcohol que desde la antigüedad se obtenía por fermentación anaeróbica de una disolución con contenido en azúcares y posterior destilación. Para obtener etanol libre de agua se aplica la destilación azeotrópica en una mezcla con benceno o ciclohexano. Otro método de purificación muy utilizado actualmente es la absorción física mediante tamices moleculares. Algunas de sus características principales son:
- Punto de ebullición: 351,6K (78ºC)
- Viscosidad: 1,074 mPa•s (20ºC)
- Solubilidad en agua: miscible
Se utiliza en el sector farmacéutico, como excipiente de algunos medicamentos y cosméticos. Es un buen disolvente, y puede utilizarse como anticongelante. También es un buen desinfectante. La industria química lo utiliza como compuesto de partida en la síntesis de diversos productos, como el acetato de etilo (un disolvente para pegamentos, pinturas, etc.), el éter dietílico, etc.
En cuanto a la peligrosidad, su punto de inflamación está en 286K (13ºC), y su temperatura de autoignición en 636K (363ºC), por lo que es inflamable a temperaturas no muy elevadas, pero se necesita una alta temperatura para que arda espontáneamente.
La exposición prolongada a concentraciones superiores a 5.000 ppm causa irritación de los ojos y la nariz, cefalea, sopor,fatiga y narcosis. El alcohol etílico se oxida muy rápidamente en el organismo a dióxido de carbono y agua. El alcohol no oxidado se excreta en la orina y en el aire espirado, de manera que apenas se producen efectos acumulativos. Su efecto en la piel es similar al de todos los disolventes de grasas y, de no tomarse las debidas precauciones, puede producirse una dermatitis de contacto. Se trata de un disolvente tóxico, afecta al sistema nervioso central.
Propanol

El propanol es un alcohol primario con fórmula C3H8O. Este líquido incoloro es también conocido como propan-1-ol, alcohol 1-propílico, alcohol n-propilo, n-propanol, o simplemente propanol. Es un isómero de isopropanol (2-propanol, alcohol isopropílico). Se forma naturalmente en pequeñas cantidades durante muchos procesos de fermentación y se utiliza como un disolvente en la industria farmacéutica principalmente para resinas y ésteres de celulosa. El propanol se obtiene de diversas maneras. Se forma como producto secundario en la síntesis de metanol. Actualmente se prepara en gran cantidad por oxidación parcial de mezclas propano-butano. Al mismo tiempo se forman otros productos, como aldehidos, metanol, isopropanol, butanoles y otros, de los cuales se separa por destilación. Algunas de sus características principales son:
- Punto de ebullición: 370,3K (97ºC)
- Viscosidad: 2,26cP
- Solubilidad en agua: miscible
Se utiliza en compuestos anticongelantes, solvente para gomas, lacas, hule, aceites esenciales, creosota. Componente en aceites y tintas de secado rápido. En productos cosméticos como son lociones y productos refrescantes. En la limpieza de aparatos electrónicos. En la fabricación de acetona, glicerina, acetato de isopropilo. En medicina como antiséptico.
En cuanto a la peligrosidad, su punto de inflamación está en 288K (15ºC), y su temperatura de autoignición en 623K (350ºC), por lo que es inflamable a temperaturas no muy elevadas, pero se necesita una alta temperatura para que arda espontáneamente. Tiene baja toxicidad, pero produce efectos a corta y larga exposición, en sistema nervioso central, sistema respiratorio y piel.
El propanol es moderadamente tóxico cuando se administra por vías respiratoria, oral o percutánea. Irrita las mucosas y deprime el sistema nervioso central. Cuando se inhala, produce una leve irritación del aparato respiratorio y ataxia. Es algo más tóxico que el isopropanol, pero aparentemente provoca los mismos efectos biológicos.
Isopropanol
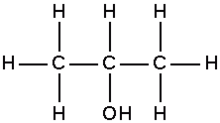
El isopropanol es un compuesto químico con fórmula molecular C3H8O o C3H7OH. Es un compuesto químico incoloro e inflamable con un olor fuerte. Es el ejemplo más simple de un alcohol secundario. Es un isómero estructural de propanol. Se encuentra en estado líquido y se obtiene por hidratación del propileno o por hidrogenación de la acetona.
Algunas de sus características principales son:
- Punto de ebullición:355 K (82ºC)
- Viscosidad: 2,08 cP (298K)
- Solubilidad en agua: muy miscible
Mezclado con agua se usa para limpieza de lentes ópticas, contactos de aparatos electrónicos, etc. También se usa para la síntesis orgánica, como intermediario químico y para disolver compuestos orgánicos como ceras o resinas.
En cuanto a la peligrosidad, su punto de inflamación está en 285K (12ºC), y su temperatura de autoignición en 736K (456ºC), por lo que es inflamable a temperaturas relativamente bajas, pero se necesita mucha temperatura para que arda espontáneamente. El isopropanol tiene una baja toxicidad, es menos irritante que el alcohol etílico, por lo que se puede sustituir por él como antiséptico con los mismos resultados. El isopropanol se metaboliza en el organismo dando acetona, que puede alcanzar concentraciones elevadas, y a su vez, es metabolizada y es excretada por los riñones y los pulmones. En el ser humano, concentraciones de 400 ppm producen irritación leve de ojos, nariz y garganta.
Butanol
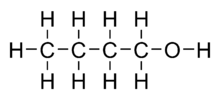
El butanol tiene una fórmula molecular de C4H10O. Se trata de un alcohol primario, que se encuentra naturalmente como subproducto de la fermentación de azúcares e hidrocarburos. Se trata de un petroquímico generalmente usado cerca de donde se produce (a partir del propileno)
Algunas de sus características principales son:
- Punto de ebullición:390.88 K (118ºC)
- Viscosidad: 2,99 cP (298K)
- Solubilidad en agua: 79g/L de agua
Su principal uso es como intermediario industrial para la fabricación de acrilato de butilo. También se usa como saborizante artificial en EEUU en alimentos como la manteca, la crema, el ron, el helado o el caramelo.
En cuanto a la peligrosidad, su punto de inflamación está en 303K (30ºC), y su temperatura de autoignición en 413K (140ºC), por lo que se trata de un líquido inflamable, y para arder de forma espontánea no necesita tanta temperatura como los anteriores. Se trata de un compuesto muy irritante para los ojos y también para la piel en períodos de contacto prolongados. La inhalación de vapores afectaría al SNC (sistema nervioso central) y tracto respiratorio.
El butanol es potencialmente más tóxico que su homólogos inferiores, pero los riesgos prácticos asociados a su producción industrial y su uso a temperatura ambiente son muy pequeños debida a su escasa volatilidad. Las altas concentraciones de vapor producen narcosis y muerte en los animales. La exposición del ser humano a los vapores puede causar irritación de las mucosas. Las concentraciones que producen irritación varían entre 50 y 200 ppm. Con más de 200 ppm pueden presentarse edema leve transitorio ocular. El contacto del líquido con la piel provoca irritación, dermatitis y absorción.
Referencias
- [13] Vale A (2007). "Methanol". Medicine 35 (12): 633–4.
- [14] "Methanol Poisoning Overview". Antizol.
- https://en.wikipedia.org/wiki/Alcohols
Enlaces externos
- Obtención de metanol
- [15] Ficha de seguridad Metanol INSST
- [16] Ficha de seguridad Etanol INSST
- [17] Ficha de seguridad Propanol INSST
- [18] Ficha de seguridad Isopropanol INSST
- [19] Ficha de seguridad Butanol INSST
- [20] Propiedades de los alcoholes INSST
Introducción
Los éteres son una familia de compuestos orgánicos que se caracteriza por la presencia del grupo funcional R-O-R', siendo R y R' grupos alquilo. Estos compuestos tienen un gran número de aplicaciones, y una de ellas es su uso como disolventes para reacciones químicas ya que son capaces de disolver a un gran número de compuestos orgánicos.
Como la mayoría de los compuestos orgánicos, son menos densos que el agua y presentan una gran hidrofobicidad. Su uso en la industria química está condicionado por su peligrosidad. Son compuestos muy volátiles y fácilmente inflamables, además son capaces de formar peróxidos (compuestos altamente reactivos) y por lo tanto siempre que se usan éteres existe un cierto riesgo de explosión[1].
MTBE

El metil tert-butil éter o, también conocido como MTBE, es un líquido de olor característico desagradable. Se fabrica mediante la combinación de sustancias químicas como el isobutileno y el metanol en un proceso de destilación reactiva a temperaturas moderadas y altas presiones. Existen otros procesos de síntesis, pero industrialmente este es el más utilizado.
Algunas de sus características principales son:
- Punto de ebullición:328.5 K (55.3ºC)
- Solubilidad en agua: 42 g/L (20ºC)
- Densidad: 0,74 g/ml (20ºC)
- Temperatura y presión críticas: 33.7 bar y 223.4ºC
Desde 1980 se usa como aditivo para aumentar el octanaje en la gasolina sin plomo[2]. También se usa para disolver cálculos biliares insertando unos tubos mediante cirugía por donde se hace llegar el MTBE directo a los cálculos.
En cuanto a la peligrosidad, su punto de inflamación está en 245K (-28ºC), y su temperatura de autoignición en 733K (460ºC), por lo que se trata de un líquido extremadamente inflamable, aunque es más difícil alcanzar la temperatura para que arda espontáneamente. Se trata de un compuesto con efecto narcótico e irritante suave en piel y ojos. Peligroso para la vida acuática.
Dietil éter
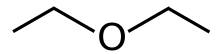
El dietil éter o éter dietílico es un líquido incoloro muy volátil con un olor característico. Se obtiene principalmente como subproducto de la hidratación de etanol a partir de etileno. En el proceso se utilizan catalizadores ácidos soportados, y si es necesario se puede aumentar el rendimiento a éter hasta un 95%[3].
- CH3CH2OH + H3O+ → CH3CH2OH2+ + H2O
- CH3CH2OH2+ + CH3CH2OH → H2O + H+ + CH3CH2OCH2CH3
Algunas de sus propiedades fisico-químicas principales son:
- Punto de ebullición: 34,6ºC
- Densidad (del líquido): 0,71 g/ml (20ºC)
- Solubilidad en agua: 6,9 g/100 ml (20 °C)
- Temperatura y presión críticas: 192,7 ºC y 35,6 bar
Debido a sus propiedades se usa principalmente como disolvente en la producción de polímeros de celulosa aunque debido a la alta peligrosidad por riesgo de explosión del dietil éter (y los éteres en general) se está tendiendo a su sustitución por otros disolventes. También se usa para la extracción de principios activos de animales y plantas debido a su fácil eliminación. Otro uso habitual del éter es el de disolvente para la síntesis de reactivos de Grignard. Por último, fue el primer producto usado como anestésico (año 1842), y se sigue utilizando como tal aunque en menor medida ya que se ha ido sustituyendo por otro tipo de compuestos tales como hidrocarbonos fluorados que presentan menos riesgos de explosión[4].
Su punto de inflamación es de -45ºC y su temperatura de autoignición es de 160ºC por lo que es un compuesto altamente inflamable y explosivo. Además, puede formar peróxidos y su vapor es menos denso que el aire por lo que se puede acumular en lugares cerrados. Las mezclas aire-éter con más de un 1,85% (en volumen) de éter son explosivamente peligrosas. La mera presencia de electricidad estática es capaz de generar un incendio en ambientes con un contenido de éter elevados. En cuanto a los riesgos para la salud humana, es moderadamente tóxico y causa síntomas de narcosis y anestesia. Puede causar la muerte por parálisis respiratoria en casos extremos. Es irritante de piel y ojos, y no es mutagénico ni carcirógeno.
THF
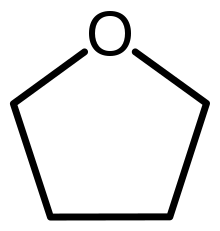
El THF o tetrahidrofurano es un líquido incoloro con un olor similar al de la acetona. En la actualidad existen varios métodos de producción industrial del THF, uno de ellos se basa en la deshidratación de 1,4-butanodiol utilizando catalizadores ácidos. Otro método desarrollado por DuPont consiste en la oxidación de n-butano a anhídrido maleico y posteriormente una reducción catalítica de este compuesto para obtener el THF[5]. Otras posibles rutas de síntesis menos utilizadas son la hidrogenación de furano o la conversión de algunos azúcares.
Algunas de sus propiedades fisico-químicas principales son:
- Punto de ebullición: 66ºC
- Densidad (del líquido): 0,89 g/ml (20ºC)
- Solubilidad en agua: miscible
- Temperatura y presión críticas: 267 ºC y 50,2 bar
El THF es un disolvente aprótico moderadamente polar que se usa industrialmente para la producción de PVC así como para barnices y en la industria farmacéutica. A nivel de laboratorio también se usa como disolvente para una amplia gama de compuestos así como para la síntesis de reactivos de Grignard y reacciones de hidroboración. También es común su uso como eluyente en cromatografía de fase reversa. Este compuesto en presencia de ácidos fuertes polimeriza formando un polímero lineal, el politetrahidrofurano. Este polímero es útil en la formación de fibras elásticas y para resinas de poliuretano. Así mismo, este polímero se usa como material de partida para la producción de polímeros termoplásticos.
- n C4H8O → -(CH2CH2CH2CH2O)n-
Su punto de inflamación es de -14,5ºC y su temperatura de autoignición es de 321ºC siendo por lo tanto un compuesto altamente inflamable y que además es capaz de formar mezclas explosivas con aire. Además, su vapor es más denso que el aire por lo que puede acumularse en sitios cerrados aumentando la peligrosidad. En cuanto a su toxicidad, presenta una toxicidad moderada. Es irritante de piel y ojos y provoca dolores de cabeza, nauseas y hasta pérdida del conocimiento por inhalación e ingestión. Presenta una ecotoxicidad baja para organismos acuáticos debido a que es biodegradable y no bioacumulable.
DME
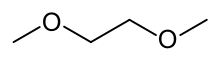
El DME o 1,2-dimetoxietano es un líquido incoloro con olor característico. Su síntesis se puede llevar a cabo por diferentes métodos. Mediante una reacción de Willamson en la que se hace reaccionar la sal de sodio de 2-metoxietanol con clorometano obteniendo como subproductos hidrógeno y cloruro de sodio.
- 2 CH3OCH2CH2OH + 2 Na → 2 CH3OCH2CH2ONa + H2↑
- CH3OCH2CH2ONa + CH3Cl → CH3OCH2CH2OCH3 + NaCl
Otra alternativa es la alquilación de 2-metoxietanol con dimetil sulfato.
El último método es la apertura del óxido de etileno con dimetil éter catalizada por un ácido de Lewis. Sin embargo, esta ruta produce una gran cantidad de subproductos y es necesaria la purificación por destilación.
- CH3OCH3 + CH2CH2O → CH3OCH2CH2OCH3
Los principales usos del DME son su uso como disolvente en reacciones químicas a nivel de laboratorio (principalmente en química organometálica en reacciones como la de Suzuki y Heck) y también se usa como un componente del disolvente de electrolitos en las baterías de litio.
Su punto de inflamación es de -2ºC y su temperatura de autoignición es de 202ºC por lo que se puede clasificar como un compuesto altamente inflamable. Forma mezclas explosivas con aire, y su vapor es más denso que el aire pudiéndose dar la ignición desde un punto distante. En cuanto a su toxicidad, causa enrojecimiento de los ojos, nauseas si es ingerido y puede absorberse a través de la piel.
REFERENCIAS
- https://en.wikipedia.org/wiki/Ether#Important_ethers
- https://www.osha.gov/dts/chemicalsampling/data/CH_271000.html
- https://www.osha.gov/dts/chemicalsampling/data/CH_223650.html
- https://www.osha.gov/dts/chemicalsampling/data/CH_240480.html
- http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=8071
Enlaces externos
- Información peróxidos
- ILPI
- Ficha de seguridad del MTBE
- Ficha de seguridad del dietil éter
- Ficha de seguridad del tetrahidrofurano
- ficha de seguridad del dimetoxietano
Bibliografía
- ↑ http://www.ciquime.org.ar/files/at001_5ho9axmd.pdf
- ↑ http://www.epa.gov/mtbe/gas.htm
- ↑ http://www.sciencedirect.com/science/article/pii/S0255270110003090
- ↑ http://books.google.es/books?id=dlGugYOOwxQC&pg=PA851&lpg=PA851&dq=dietil+eter+anestesico&source=bl&ots=WqA6hMVxOj&sig=tHdMGkx8rLjjC_8pWn1aHQ3-vhM&hl=es&sa=X&ei=P3BKU6OkEc2W0QWYlYHgAg&ved=0CFUQ6AEwBA#v=onepage&q=dietil%20eter%20anestesico&f=false
- ↑ http://web.archive.org/web/20110715025548/http://www.chemsystems.com/reports/search/docs/abstracts/0607_4_abs.pdf
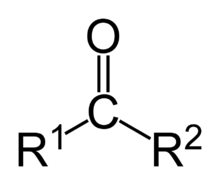
Una cetona es un compuesto orgánico caracterizado por poseer un grupo funcional carbonilo unido a dos sustituyentes constituidos por átomos de carbono, a diferencia de un aldehído, en donde el grupo carbonilo se encuentra unido al menos a un átomo de hidrógeno. Como disolventes, las cetonas son clasificadas como disolventes polares apróticos. La polaridad del grupo carbonilo también las convierte en aceptoras de puentes de hidrógeno, pero no en donoras, lo que impide la "asociación" de las moléculas. Esto supone una mayor volatilidad de las cetonas respecto a alcoholes o ácidos carboxílicos de peso molecular comparable, que aunque lógicamente implica una solubilidad en agua menor, explica la perseverancia en su uso como disolventes y en perfumería. También se usan como precursores poliméricos y en la industria farmacéutica. Las cetonas más ampliamente utilizadas son la acetona, la metil etil cetona y la ciclohexanona.
Acetona

La acetona o propanona es el compuesto orgánico de fórmula molecular (CH3)2CO, y la más simple de las cetonas. A temperatura ambiente, se trata de un líquido incoloro de olor característico, volátil e inflamable. Se obtiene a escala industrial mediante hidrólisis catalítica en medio ácido del hidroperóxido de isopropilbenceno (que se obtiene mediante la alquilación de benceno con propileno, seguida por un proceso de oxidación), que permite también la obtención de fenol (ruta del cumeno).
Otras posibles vías son:
- Deshidrogenación catalítica de isopropanol
- Fermentación
- Oxidación de propileno (proceso Hoechst-Wacker), polipropileno y diisopropilbenceno.
Algunas de sus propiedades físico-químicas son las siguientes:
- Punto de ebullición: 329.3 K (56ºC)
- Punto de fusión: 178.7 K (-94ºC)
- Punto de inflamación: 255.15 K (-18ºC)
- Temperatura de autoignición: 738.15 K (465ºC)
- Solubilidad en agua: soluble
- Densidad: 0.8 g/cm3
- Coeficiente de reparto octanol/agua: log Pow = -0.24
La acetona como disolvente supone el 17% de la producción total, el resto se destina para la producción de MMA (metil metacrilato) y PMMA (polimetilmetacrilato) usados en construcción (42%), Bisfenol-A para automóviles y microelectrónica (24%), derivados del aldol (13%), y otros (4%).
En cuanto a la peligrosidad, su punto de inflamación está en 255 K (-18ºC), y su temperatura de autoignición en 738 K (465ºC), por lo que se trata de un líquido extremadamente inflamable, aunque es difícil alcanzar la temperatura para que arda espontáneamente, muy parecido al MTBE. Se trata de un compuesto que produce irritación respiratoria al ser inhalado, pudiendo llegar a la pérdida de conocimiento, y también irrita la piel y los ojos. Su ingestión puede producir náuseas y vómitos.
Metil Etil Cetona

La metil etil cetona, también conocida como butanona o MEC, tiene una fórmula molecular de C4H8O. A temperatura ambiente, se presenta en forma de líquido incoloro inflamable, de olor característico, dulzón y penetrante. Existen dos procesos fundamentales para su obtención: el primero consiste en la deshidrogenación catalítica del alcohol sec-butílico a 250-330ºC, en presencia de cobre, zinc o bronce. El segundo proceso, denominado proceso Hoechst-Wacker, se trata de una oxidación con aire del 1-buteno en presencia de una disolución acuosa de cloruros metálicos.
Algunas de sus características principales son:
- Punto de ebullición:353 K (80ºC)
- Punto de fusión: 186.5 K (-86ºC)
- Punto de inflamación: 264.15 K (-9ºC)
- Temperatura de autoignición: 778.15 K (505ºC)
- Solubilidad en agua: 27-29g/100mL de agua (20ºC)
- Densidad: 0.805 g/cm3
- Coeficiente de reparto octanol/agua: log Pow = 0.29
Su aplicación principal es como disolvente universal de nitro- y acetilcelulosas, resinas vinílicas, cauchos clorados y celuloides, en la industria de lacas y pegamentos; así como para la desparafinación de los aceites pesados.
En cuanto a la peligrosidad, su punto de inflamación está en 264K (-9ºC), y su temperatura de autoignición en 778K (505ºC), por lo que se trata de un líquido extremadamente inflamable, aunque es más difícil alcanzar la temperatura para que arda espontáneamente, también muy parecido al MTBE. Los efectos tóxicos son similares a los provocados por la acetona.
Metil Isobutil Cetona

La metil isobutil cetona, también conocida como MIBK, es un líquido incoloro que tiene una fórmula molecular de C6H12O. Se obtienen millones de kilogramos a partir de acetona mediante tres reacciones: una condensación aldólica, para dar un alcohol diacetona; una deshidratación, para dar un óxido de mesitilo y por último una reacción con hidrógeno en presencia de Pd para dar MIBK:
Algunas de sus características principales son:
- Punto de ebullición: 390 K (117ºC)
- Punto de fusión: 187.8 K (-84.7ºC)
- Punto de inflamación: 290.15 K (17ºC)
- Temperatura de autoignición: 732.15 K (459ºC)
- Solubilidad en agua: 1.91g/100mL de agua (20ºC)
- Densidad: 0.802 g/cm3
- Viscosidad: 0.58 cP (20ºC)
Se emplea para el desparafinado de aceites lubricantes, como base o componentes de pinturas, esmaltes, lacas, barnices, selladores, diluyentes, etc. También es común su uso como tensioactivo de tintas, pinturas y pesticidas. Otros usos serían las extracciones líquido/líquido o sólido/líquido.
En cuanto a la peligrosidad, su punto de inflamación está en 290K (17ºC), y su temperatura de autoignición en 732K (459ºC), por lo que se trata de un líquido no muy inflamable, siendo difícil alcanzar la temperatura para que arda espontáneamente. Los vapores causan irritación de las vías respiratorias y los ojos teniendo como efecto bronquitis, deshidratación y efectos sobre el sistema nervioso central.
Ciclohexanona


La ciclohexanona, molécula cíclica compuesta de seis átomos de carbono y con un grupo funcional cetona, pertenece al grupo de las cetonas cíclicas, y se trata de un líquido incoloro, cuyo olor recuerda al de la acetona. La síntesis industrial de la ciclohexanona tiene lugar principalmente a través de dos procesos:
- Oxidación catalítica de ciclohexano con oxígeno atmosférico, que transcurre a través de un hidroperoxiciclohexano (o hidroperóxido de ciclohexilo) inestable, el cual vía un mecanismo radicalario da lugar a una mezca de ciclohexanona y ciclohexanol. La mezcla a continuación se separa por destilación, y el ciclohexanol aislado puede seguidamente oxidarse a más ciclohexanona.
Algunas de sus propiedades físico-químicas son las siguientes:
- Punto de ebullición: 428.8 K (155.6ºC)
- Punto de fusión: 242.15 K (-31ºC)
- Punto de inflamación: 317.15 K (44ºC)
- Temperatura de autoignición: 697.15 K (420ºC)
- Solubilidad en agua: 8.7g/100mL de agua (20ºC)
- Densidad: 0.9478 g/cm3
- Coeficiente de reparto octanol/agua: log Pow = 0.81
La ciclohexanona se emplea como disolvente en la industria, y como reactivo en la producción de ácido adípico y de caprolactama, compuestos empleados en la fabricación de nylon-6,6 y nylon-6 respectivamente. También es usado en la fabricación de PVC y como pegamento para unir partes o trozos de PVC y nylon-6,6.

En cuanto a la peligrosidad, su punto de inflamación está en 317K (44ºC), y su temperatura de autoignición en 697K (420ºC), por lo que se trata de un líquido no muy inflamable, siendo difícil alcanzar la temperatura para que arda espontáneamente. Los vapores causan irritación de las vías respiratorias y los ojos teniendo como efecto bronquitis, deshidratación y efectos sobre el sistema nervioso central.
REFERENCIAS
- Martínez Grau, M.ª Ángeles, G. Csákÿ, Aurelio (2001). «3». Técnicas experimentales en síntesis orgánica. España: SÍNTESIS. ISBN 84-7738-605-6.
Enlaces externos
- Ficha de seguridad de acetona
- Ficha de seguridad de metil etil cetona
- Ficha de seguridad de ciclohexanona
- Web del NIST
Introducción
Los ésteres, se forman a partir de la reacción entre un ácido carboxílico y un alcohol en medio ácido. A diferencia de los ácidos, no pueden donar enlaces de hidrógeno puesto que no tienen un átomo de hidrógeno unido a un átomo de oxígeno. Sin embargo, pueden aceptar enlaces de hidrógeno; así, los ésteres de baja masa molecular son solubles en agua y los de mayor masa molecular son insolubles.

Además, los aromas específicos de muchas flores y frutos se deben a la presencia de ésteres. Estos se emplean en la fabricación de perfumes y como agentes saborizantes en las industrias de la confitería y bebidas no alcohólicas. Los vapores de los ésteres son inocuos, a menos que se inhalen grandes concentraciones. El uso más importante es como disolventes industriales. Son disolventes bastante inertes, poco ionizantes y poco polarizables. En concentraciones elevadas presentan una acción anestésica. En conjunto, la mayoría de los ésteres alifáticos y aromáticos utilizados en la industria son poco tóxicos. Los ésteres, constituyen una importante categoría de disolventes para la industria de pinturas, tintas, en perfumería, cosmética y farmacia. Fueron los primeros disolventes de las resinas nitrocelulósicas y son excelentes disolventes para un gran número de resinas naturales y sintéticas no envejecidas. Los acetatos son los más utilizados, sobre todo el acetato de etilo que se adiciona comúnmente al alcohol, por ejemplo, para disolver el acetato de celulosa (5-30%) y las resinas naturales. Los propionatos presentan una volatilidad más débil que la de los acetatos y un poder de solvatación ligeramente inferior. Pueden ser útiles para fabricar barnices que deben secarse en atmósfera húmeda, ya que evitan la condensación de agua.
Propiedades químicas y físicas
A continuación, se muestran las principales reacciones que llevan a cabo los ésteres.
En cuanto a las propiedades físicas, cabe destacar:
- Los ésteres no pueden donar enlaces de hidrógeno. Esto influye en que los puntos de ebullición y fusión de los ésteres son menores en comparación a los ácidos carboxílicos con masas moleculares parecidas.
- Los ésteres son capaces de aceptar enlaces de hidrógeno, esto permite que los ésteres de baja masa molecular sean solubles en agua y los de mayor masa molecular insolubles. Los ésteres son solubles en la mayoría de los disolventes orgánicos, su solubilidad la determina la longitud de la cadena hidrocarbonada.
- Poseen olores agradables. Los aromas de muchas flores y frutos se dan gracias a la presencia de ésteres.
- La mayor parte son líquidos, incoloros, insolubles y más ligeros que el agua.
- Su viscosidad es alta
- Son aislantes eléctricos cuando se encuentran en disolución.
- Son neutros ya que estos son el resultado de la neutralización de un ácido.
Acetato de metilo

El acetato de metilo es un líquido inflamable con un olor agradable. Sus características son muy similares al del acetato de etilo
| Propiedad | Valor |
|---|---|
| Fórmula molecular | C3H6O2 |
| No CAS | 79-20-9 |
| Masa molecular | 74.1 g/mol |
| Punto de ebullición | 57 °C |
| Punto de fusión | -98 °C |
| Densidad relativa | 0.93 g/cm3 |
| Solubilidad en agua | 24.4 |
| Presión de vapor (kPa, 20 °C) | 21.7 |
| Punto de inflamación | -13 °C |
| T de autoignición | 455 °C |
| Coeficiente de reparto (Pow) | n.d |
Es un líquido incoloro, fácilmente inflamable. Irrita los ojos. La exposición repetida puede provocar sequedad o formación de grietas en la piel. La inhalación de vapores puede provocar somnolencia y vértigo. Se utiliza como un disolvente de colas y quitaesmalte de uñas, en reacciones químicas y para extracciones, también se usa para lacas, resinas, aceites, y nitrocelulosa, en pintura, como un agente aromatizante, y en la fabricación de cuero artificial.
Acetato de etilo

El acetato de etilo, o también conocido como etanoato de etilo, tiene una fórmula molecular de C4H8O2, es un líquido incoloro que se obtiene mediante la esterificación directa de Fischer con ácido acético y etanol usando catalizador.
| Propiedad | Valor |
|---|---|
| Fórmula molecular | C3H6O2 |
| No CAS | 109-94-4 |
| Masa molecular | 74.1 g/mol |
| Punto de ebullición | 77 °C |
| Punto de fusión | -84 °C |
| Densidad relativa | 0.9 g/cm3 |
| Solubilidad en agua | Muy buena |
| Presión de vapor (kPa, 20 °C) | 10 |
| Punto de inflamación | 7 °C |
| T de autoignición | 427 °C |
| Coeficiente de reparto (Pow) | 0.73 |
Se trata de un disolvente universal, en la industria química se usa como reactivo. También es usado en la industria textil, papelera, cosmética, alimenticia, etc. En el laboratorio se usa para cromatografía líquida y extracción. Muy importante para la síntesis de la vitamina E. Generalmente, se usa para la extracción líquida de antibióticos, en la industria de pinturas se ocupa como disolvente activo para disolver las resinas sintéticas ocupadas en la formulación de estas.
En cuanto a la peligrosidad, su punto de inflamación está en 280K (7ºC), y su temperatura de autoignición en 700K (427ºC), por lo que se trata de un líquido extremadamente inflamable, pero es más difícil alcanzar la temperatura para que arda espontáneamente. Requiere ventilación adecuada. Irrita la piel y las vías respiratorias, produce debilidad, vértigo, somnolencia, dolor de cabeza, etc.
Acetato de isopropilo
Es un líquido incoloro que reacciona violentamente con materiales oxidantes. Ataca a muchos plásticos. Se puede absorber por inhalación del vapor o por ingestión. En la evaporación de esta sustancia a 20ºC se puede alcanzar rápidamente una concentración nociva en el aire.
Algunas de sus características principales son:

Se utiliza como disolvente para plásticos, aceites y grasas, y como agente aromatizante.
Acetato de n-butilo

El acetato de butilo, o también conocido como BAC, butil acetato, ester butílico o etanoato de butilo, tiene una fórmula molecular de C6H12O2 es un líquido incoloro y transparente de olor frutal que se obtiene por esterificación directa del ácido acético con alcohol butílico en presencia de un catalizador.
Algunas de sus características principales son:

Debido a su gran poder disolvente, el acetato de butilo, es muy utilizado en las industrias de tintas y barnices y muchos tipos de revestimientos y acabados. También como ingrediente de sabores y esencias frutales. Otros usos son como disolvente de resinas sintéticas, acrílicas, polivinilacetatos, cetónicas y aldehídicas.
En cuanto a la peligrosidad, su punto de inflamación está en 295K (22ºC), y su temperatura de autoignición en 633K (360ºC). Sus vapores forman con el aire mezclas inflamables o explosivas a temperatura ambiente. Irrita las mucosa y sistema respiratorio, piel y ojos, produciendo daño en los tejidos y conjuntivitis en los ojos.v Los efectos narcóticos de acetato de n-butilo es mayor que los ésteres de alquilo. También, las toxicidades y acciones irritantes son algo mayor que isopropilo, y acetatos de etilo.
Se utiliza en la fabricación de lacas, plásticos, películas fotográficas, y cueros artificiales.
Usos generales en la industria
- Disolventes: Los ésteres de bajo peso molecular son líquidos y se acostumbran a utilizar como disolventes, especialmente los acetatos de los alcoholes metílico, etílico y butílico, ya citados anteriormente.
- Plastificantes: El acetatopropionato de celulosa y el acetatobutirato de celulosa han conseguido gran importancia como materiales termoplásticos.
- Aromas artificiales: Muchos de los ésteres de bajo peso molecular tienen olores característicos a fruta: plátano (acetato de isoamilo), ron (propionato de isobutilo)… Se utilizan en la fabricación de aromas y perfumes sintéticos.
- Aditivos alimentarios: Los ésteres de bajo peso molecular tienen olores característicos a fruta, se utilizan como aditivos alimentarios, por ejemplo, en caramelos y otros alimentos que han de tener un sabor afrutado. Se usan para quitar la cafeína de los granos de café y de las hojas de té en la industria alimentaria.
- Productos farmacéuticos y medicina: Productos de uso tan frecuente como los analgésicos se fabrican con ésteres. Los ésteres del ácido salicílico se utiliza en medicina; la común aspirina es ácido acetil salicílico, el salicitato de metilo y el salicilato de fenilo.
- Polímeros: Algunos ésteres son inestables y polimerizan rápidamente produciendo resinas, metacrilato de metilo. También dada su inestabilidad pueden reaccionar con ellos mismos; por ejemplo el acetato de polivinilo…
- Repelentes de insectos: Todos los repelentes de insectos que podemos encontrar en el mercado contienen ésteres.
Impacto en el medio ambiente y en la salud humana
En general el uso de esteres, tanto para el medio ambiente como para la salud humana, tiene un efecto negativo.
Los ésteres de ftalatos, principalmente conocidos como plastificantes, son un grupo de productos químicos industriales utilizados para la fabricación de plásticos más flexibles, como el PVC. Hoy en día, se considera que por su elevada toxicidad, volatilidad y persistencia en el medio, la exposición ambiental a los ésteres ftalatos es uno de los más probables responsables de ocasionar enfermedades como cáncer, malformaciones congénitas, pérdida de calidad en el semen masculino y esterilidad, además de ser uno de los principales contaminantes de la atmósfera por su participación en reacciones fotoquímicas.
Lo anterior, se ha dado debido a que hoy en día la utilización de este tipo de ésteres se ha expandido a la fabricación de juguetes, envases de alimentos, lubricantes, detergentes, pesticidas, cosméticos, y en general productos con los que tenemos contacto diario, lo que ocasiona que al tocar nuestra piel sea fácilmente absorbido. Sin embargo, los ésteres de ftalatos son utilizados por su bajo coste, aunque en países como los de la Unión Europea, estas sustancias químicas han sido prohibidas por sus efectos nocivos.
En elevada concentración, los esteres presentan una acción anestésica. El acetato de metilo libera metanol en el organismo. En conjunto, la mayoría de los ésteres alifáticos y aromáticos utilizados en la industria son poco tóxicos, lo que los hace muy útiles.
Referencias
- Pradyot Patnaik, "A Comprehensive guide to the hazardous properties of chemical substances"
Enlaces externos
- Acetato de butilo
- Aplicaciones del acetato de butilo
- Disolventes industriales: Ésteres[21]
- CRC Handbook of Lubrication and Tribology, Volume III[22]
- Ficha Técnica: Acetato de metilo[23]
- Ficha Técnica: Acetato de etilo[24]
- Ficha Técnica: Acetato de isopropilo [25]
- Ficha Técnica: Acetato de n-butilo [26]
{{:Disolventes en la Industria Química
/Amidas|Amidas}}
Acetonitrilo
El acetonitrilo, tiene una fórmula molecular de C2H3N. se obtiene como subproducto en la fabricación de acrilonitrilo. Las rutas de obtención son la deshidratación de acetamida o hidrogenación de mezclas de monóxido de carbono y amoniaco.
Algunas de sus características principales son:
- Punto de ebullición:355 K (82 °C)
- Solubilidad en agua: miscible
- Densidad: 0,786 g/cm3
Se usa principalmente como disolvente en la purificación de butadieno en las refinerías. También se usa en aplicaciones de baterías, ya que posee una elevada constante dieléctrica y disuelve electrolitos. En el laboratorio puede usarse para HPLC. Desempeña un papel significativo como disolvente dominante en la fabricación de monómeros del ADN.
En cuanto a la peligrosidad, su punto de inflamación está en 286K (13 °C), y su temperatura de autoignición en 797K (524 °C), por lo que se trata de un líquido inflamable, pero es más difícil alcanzar la temperatura para que arda espontáneamente. Con la exposición al acetonitrilo, puede ser metabolizado a HCN, que es el causante de dificultades en la respiración, pulso lento, náuseas y vómitos.
REFERENCIAS
Enlaces externos
Referencias
| ||||||||||||||||||||||||||||||||||||||||||||
El disulfuro de carbono (CS2) puro es un líquido incoloro volátil a temperatura ambiente, con un olor dulce agradable. Sin embargo, el disulfuro de carbono impuro que se suele usar en la mayoría de los procesos industriales es un líquido amarillento que tiene un olor desagradable. Este compuesto suele usarse frecuentemente como molécula ladrillo para síntesis orgánica, y como disolvente apolar.
Síntesis
Se puede encontrar CS2 en la naturaleza de manera natural proveniente de gases liberados a la atmósfera, por ejemplo, en erupciones volcánicas. Comercialmente, se encuentra como una mezcla azeotrópica con agua que contiene 97.2% de CS2.
El disulfuro de carbono se produce comercialmente mediante la reacción de azufre y carbón o metano. El CS2 fue fabricado por primera vez, en torno a 1880. Hasta aproximadamente 1950, el método de producción a escala industrial era calentando carbón a 750 – 900ºC en presencia de azufre vaporizado. Sin embargo, se siguió investigando otros métodos de producción y en 1965 el método de la quema de carbón quedó en gran parte reemplazado por la reacción del azufre con gas natural que contiene hidrocarburos, tales como metano, etano o etileno. Ésta reacción se lleva a cabo a 550-650ºC y a una presión de 400-700 kPa con un catalizador de sílice o alúmina. En lugares en los que el metano o gas natural no se encuentran disponible, o cuando se trata de una planta pequeña, el proceso con carbón todavía se utiliza.[1]
2CH4 + S8 → 2CS2 + 4H2S
Peligrosidad
El disulfuro de carbono presenta un índice alto de peligrosidad. Es una sustancia altamente inflamable. Muchas reacciones pueden producir incendio o explosión, además en caso de incendio se desprenden humos tóxicos e irritantes. Las mezclase vapor/aire son explosivas, los límites de explosión son 1,3-50%.[2]
Efectos tóxicos
Esta sustancia puede absorberse tanto por inhalación, absorción cutánea e ingestión. Puede provocar vértigo, dolor de cabeza, náuseas, jadeo, vómitos, debilidad, irritabilidad, alucinaciones. En contacto con la piel puede provocar enrojecimiento. La cantidad de disulfuro de carbono que se encuentra en el aire de manera natural no supone un peligro para la salud ni el medio ambiente. Los trabajadores de las plantas que usan el disulfuro de carbono en sus procesos de producción son los más expuestos a esta sustancia. La principal ruta de exposición es el aire y la secundaria, la piel. Aproximadamente del 10 al 30% del disulfuro de carbono que el cuerpo absorbe sale por los pulmones y menos del 1% por la orina. El resto del disulfuro de carbono absorbido se metaboliza en el cuerpo y sale por la orina en forma de otra sustancia química. También se puede excretar el CS2 en pequeñas cantidades por el sudor y la saliva. A niveles muy altos, 10000ppm, el disulfuro de carbono puede poner en peligro la vida de las personas debido a las consecuencias que provoca en el sistema nervioso. Estudios realizados en animales muestran que, a altos niveles, el CS2 puede afectar el corazón. Los trabajadores no deberían estar expuestos a más de 20 ppm para una jornada laboral de 8 horas diarias durante 5 días a la semana (estudio según la OSHA, Administración de Seguridad y Salud Ocupacionales). Estudios realizados en animales indican que el disulfuro de carbono puede afectar las funciones normales del cerebro, el hígado y el corazón. La EPA indica que ingerir o absorber diariamente una cantidad equivalente a 0.1 mg de disulfuro de carbono por kg de peso corporal probablemente no cause efectos adversos significativos a la salud.[3]
Uso en la industria
Varias industrias usan el disulfuro de carbono como materia prima para fabricar rayón, celofán o tetracloruro de carbono. En la actualidad, la industria que más utiliza esta sustancia es del rayón viscosa. El disulfuro de carbono también se utiliza para disolver el caucho para producir llantas y como materia prima para producir pesticidas.
El disulfuro de carbono ha sido un químico industrial importante desde los años ochenta debido a sus muchas propiedades útiles, incluyendo su capacidad de solubilizar grasas, cauchos, fósforo, azufre y otros elementos. Las propiedades de disolver del disulfuro de carbono lo hacen indispensable en la preparación de grasas, lacas y alcanfor, en la industria refinadora de petróleo y en parafinas. Además, lo han hecho altamente apropiado para una gran variedad de aplicaciones industriales incluyendo: vulcanización y manufactura de cauchos y accesorios de caucho; producción de resinas, xantatos, tiocianatos, adhesivos para madera y agentes de flotación; inhibidor en la polimerización de cloruro de vinilo; en la conversión y procesamiento de hidrocarburos; purificación de petróleo; brillo de metales preciosos en galvanoplastia; como un agente para incrementar la resistencia a la corrosión y el desgaste de metales; removedor de óxido de metales y para la remoción y recuperación de metales y otros elementos de aguas de desecho y otros medios.
Asia, incluyendo Japón, representaron alrededor del 72% de la producción mundial de CS2 y casi el 75% del consumo mundial de disulfuro de carbono. China es el jugador dominante mundial en esta industria, con alrededor del 49% del consumo mundial, seguido por la India (13%). En total, el 98% del consumo mundial de disulfuro de carbono correspondió a Asia, Europa y América.[4]
 |
Impacto económico
La mayor parte de disulfuro de carbono que se utilizaba hasta 1980, era para la obtención de tetracloruro de carbono. Sin embargo, debido al Protocolo de Montreal en 1978, la demanda de disulfuro de carbono en la producción de tetracloruro de carbono se redujo considerablemente. Otros usos muy importantes del disulfuro de carbono, son sus usos para aplicaciones agrícolas. En 2007, el 44% de la demanda de disulfuro de carbono se utilizaba para la fabricación de productos agrícolas. En concreto, una de las áreas de consumo más grandes de los productos químicos agrícolas es en la fabricación de ditiocarbamatos, que se utiliza como fungicidas, biocidas y fumigantes.
La fabricación de fibras de rayón y caucho también es un sector importante que representa aproximadamente el 24% de la demanda. El rayón se utiliza en prendas de vestir, artículos del hogar, telas, tejidos y en diversas aplicaciones industriales. Si bien es verdad, en los últimos años la demanda de rayón ha comenzado a disminuir, entre 1994 y 2004 el consumo de CS2 para la fabricación de rayón se redujo en casi un 9%/año y más recientemente un 5%/año. Esta disminución se debe a la utilización de mezclas de fibras con el fin de reducir los costos.
La industria del caucho requiere el CS2 para la fabricación de aceleradores de la vulcanización. El mercado de aceleradores de vulcanización es paralela a la de los neumáticos, y se prevé que continúe creciendo en torno al 1.5%/año.
El precio del CS2 ha ido aumentando con el paso de los años como se puede ver en la gráfica de abajo. Son datos del precio de CS2 en Estados Unidos.[5] El precio de CS2 en pequeña cantidad está en torno a 60€/l.[6]
 |
Impacto ambiental
Como ya se ha comentado, en la naturaleza se encuentran pequeñas cantidades de disulfuro de carbono en los gases liberados a la superficie terrestre. Algunos microorganismos presentes en el suelo, en lagos o pantanos pueden liberarlo también. El CS2 se evapora rápidamente cuando es liberado al medio ambiente. Es difícil juzgar la cantidad de disulfuro de carbono que es liberado al aire mediante procesos artificiales debido a que el disulfuro de carbono se encuentra en la naturaleza en cantidades muy pequeñas. Una vez liberado al medio ambiente, el disulfuro de carbono se disuelve rápidamente en el aire. Cuando está en el aire, permanece cerca del suelo debido a que es más pesado que el aire circundante. Se estima que se degrada totalmente en unos 12 días. Debido a que esta sustancia química no se adhiere fuertemente a los suelos, la cantidad que no se evapora puede desplazarse fácilmente por los suelos hasta llegar a las aguas subterráneas.[7]
Sustitución por otros disolventes
El disulfuro de carbono es ampliamente utilizado en determinadas aplicaciones por su capacidad para disolver determinadas sustancias como resinas, gomas, fósforo y rayón. Sin embargo, el disulfuro de carbono es uno de los disolventes más peligrosos. Cuenta con un amplio rango inflamable, y una temperatura de autoignición de 90ºC, siendo capaz de incendiarse en contacto con superficies calientes o con agua caliente. Además, la exposición crónica a vapores de disulfuro de carbono pueden conducir a diversas enfermedades que afectan al cerebro, corazón, riñón, hígado y ojos. Por este motivo, se están investigando disolventes que puedan sustituir al CS2 en determinadas aplicaciones. Por ejemplo, se ha visto que para la extracción de alcanos un disolvente que también presenta buen rendimiento es el diétil éter.[8]
Referencias
- ↑ Documentación general del CS2
- ↑ Toxnet
- ↑ "Chemical Summary for Carbon Disulfide" EPA 749-F-94-008a
- ↑ "Carbon Disulfide report from IHS Chemical" Retrieved June 15, 2013.
- ↑ "ICIS Chemical Business". 8 Sep 2008.
- ↑ Sigma Aldrich, carbon disulfide
- ↑ "PubChem. Compound CS2" CID 6348
- ↑ Comparison of the Eluting Efficiency of Carbon Diethyl Ether: The Case for Laboratory Safety. John J. Lentini, B.A. and Andrew T. Armstrong, Ph.D.
La industria farmacéutica tiene como objetivo la producción de compuestos con actividad farmacológica. Los fármacos son productos complejos que requieren numerosas etapas de síntesis, y por tanto generan una gran cantidad de residuos.
Las principales rutas de obtención de fármacos son: la síntesis biológica, la síntesis química y la extracción de productos naturales. Después de la obtención del principio activo se requieren numerosos pasos de extracción, purificación y acondicionamiento. Pese a que para estos pasos se requieren grandes cantidades de disolventes, la cantidad de residuos que este tipo de industrias produce es bastante baja debido a que no se producen grandes cantidades de producto, aunque si lo referimos a la cantidad de residuos producidos por unidad de masa de producto (factor e) vemos la necesidad de mejora en los procesos.
Tabla del factor e según la industria [1]
| sector industrial | producción (ton) | factor e |
| petroquímica | 106-108 | <0.1 |
| commodities | 104-106 | <1–5 |
| química fina | 102−104 | 5–50 |
| farmacéutica | 10–103 | 25–100 |
Los disolventes se usan en cantidades mayores que el producto de interés que se quiere obtener, y pese a que pueden llegar a recuperarse entre un 50 y un 80% de la cantidad usada, suponen la mayoría de los vertidos de esta industria, normalmente entre un 80 y un 90% del total de los residuos.
Disolventes tradicionales
Los disolventes que tradicionalmente se han usado en la industria farmacéutica han sido disolventes orgánicos como el THF, diclorometano o tolueno. Sin embargo en los últimos años se ha hecho un esfuerzo por parte de las empresas para la disminución de la cantidad de disolventes usados, y por la sustitución [2] de estos por otros menos peligrosos como por ejemplos alcoholes, aunque no siempre la sustitución es posible por la implicación del disolvente en el mecanismo de reacción.
Los disolventes más usados en la industria farmacéutica son:
- alcoholes: etanol, butanol, 2-etilhexanol, isobutanol, isopropanol, metanol, propanol y propilenglicol
- cetonas: acetona, 2-butanona, metil isobutil cetona, metil isopropil cetona y isobutenil metil cetona
- halogenados: tricloroetileno, bromuro de etileno, cloroformo, cloruro de etileno, diclorometano, tetracloro etileno y tetracloruro de carbono
- amidas: dimetilformamida
- éteres: 1,4-dioxano, dibutil eter, eter etílico, diisopropileter, tetrahidrofurano y ter-butil metil eter
- disolventes con azufre: dimetilsulfóxido
- aminas: piridina
- nitrilos: acetonitrilo
- ésteres: acetato de etilo
- hidrocarburos alifáticos: ciclohexano y hexano
- agua
- hidrocarburos aromáticos: tolueno y xileno
Nuevos disolventes
Se están investigando disolventes más benignos con el medio ambiente y seguros como fluidos supercríticos, líquidos iónicos, medios acuosos y síntesis sin disolventes para disminuir el impacto ambiental de esta industria. Se espera que en un futuro los disolventes neotéricos ayudarán en la sostenibilidad de la industria farmacéutica, aunque por el momento aún requieren más investigaciones para hacer procesos más rentables y más investigaciones sobre su posible toxicidad.
fluídos supercríticos
La gran mayoría de los medicamentos presentan una forma cristalina. El proceso de cristalización es una etapa importante en la industria farmacéutica porque puede ejercerse un control sobre el tamaño y forma de los cristales, lo que influye en sus características para ser absorbidos por el organismo. Además, debido al propio uso de los medicamentos, existen rigurosas limitaciones a la cantidad de disolventes que pueden quedar en el medicamento, por lo que un disolvente fácil de eliminar como los fluidos supercríticos puede aportar seguridad al medicamento.
Las aplicaciones[3] de los fluidos supercríticos no solo se limitan a las cristalizaciones, sino que también pueden usarse en extracciones (muy comunes también en este tipo de industrias), como disolvente, para micronización, agente para nebulizaciones, etc.
Uso de disolventes
El proceso para fabricar un medicamento pasa por varios pasos que se engloban en tres pasos: La obtención del principio activo, la formulación y el empaquetado. En ellos es necesario que el disolvente además de cumplir su papel, pueda ser removido del medicamento en la medida de lo posible para evitar toxicidad, y si se puede, ser reciclado.
Obtención del principio activo
La obtención del principio activo es un proceso multietapa en el que este se sintetiza químicamente o se obtiene por medios bioquímicos, se separa y se purifica, normalmente por cristalización.
Durante la síntesis el disolvente actúa como medio de reacción, poniendo en contacto los distintos reactivos solubilizándolos. En esta parte las propiedades del disolvente pueden modificar los mecanismos y velocidad de reacción y alterar la selectividad del proceso.
En la parte de cristalización el disolvente puede afectar a la forma y tamaño de los cristales, y por tanto a las propiedades de solubilidad y farmacocinética. Cuando la cristalización ha finalizado es necesario eliminar los restos de disolvente mediante un secado, pero sin dañar los cristales formados. Existe una rigurosa legislación que limita la cantidad de disolvente que puede quedar en función de su peligrosidad.
formulación

La formulación es el proceso por el cual el principio activo se prepara en función de la vía de administración. En este proceso puede interesar que quede disolvente como forma de solubilizar medicamentos líquidos o semisólidos cuando el agua no es una opción. Además del principio activo, el disolvente debe ser capaz de disolver otros compuestos como estabilizantes, antioxidantes, antimicrobianos, etc. Los medicamentos que se producen en forma sólida también necesitan de disolventes para poder tenerlos en la forma deseada, granulada, en tabletas, encapsulados, etc.
Seguridad
En la industria farmacéutica se llevan a cabo numerosas etapas de muy distinto tipo. Según la ruta que se lleve use para obtener el fármaco se deberán tomar unas medidas de seguridad u otras.
síntesis por fermentación
La síntesis mediante rutas fermentativas requiere el uso de microorganismos para la producción del principio activo, lo que supone trabajar en un medio acuoso. En este caso el riesgo del uso de disolventes es bajo debido a la poca toxicidad del agua y al uso de microorganismos no patógenos, aunque los trabajadores deben de tener cuidado en etapas en las que se usa vapor de agua caliente o productos químicos para la desinfección de la maquinaria. Así mismo, en etapas posteriores de síntesis y extracción los peligros de toxicidad e inflamabilidad de disolventes orgánicos se ven reducidos por la dilución en agua.
síntesis química
En las síntesis químicas de los productos farmacéuticos existe un peligro mayor que en una síntesis biológica o en una extracción debido a la peligrosidad de los reactivos y solventes orgánicos. Estos pueden producir efectos agudos sobre la salud, pueden dañar los ojos y la piel y ser corrosivos o irritantes, provocar sensibilización o reacciones alérgicas o ser asfixiantes. Los productos químicos con efectos crónicos sobre la salud pueden provocar cáncer, alteraciones en órganos como el hígado, riñones o pulmones, o afectar los sistemas nervioso, endocrino, reproductor u otros órganos. Los riesgos para la salud y la seguridad de los trabajadores se pueden controlar aplicando las medidas de control adecuadas (p. ej., modificaciones del proceso, controles técnicos, prácticas administrativas, equipo de protección personal y respiratoria). Además Las reacciones de síntesis orgánica pueden provocar riesgos debido a su inflamabilidad y a la posibilidad de explosiones. Todos estos riesgos no solo pueden afectar a los trabajadores de la propia planta, sino que pueden afectar también a la población establecida en los alrededores de la planta y a los consumidores si no se eliminan adecuadamente los disolventes de los medicamentos.
extracción biológica o natural
En la extracción biológica se extraen los compuestos activos principalmente de plantas. Se han de tomar medidas similares a las tomadas en el caso de la síntesis química. El uso de disoluciones ácidas o básicas para neutralizar en etapas de extracción supone uno de los riesgos principales en este tipo de rutas. Así mismo, hay que tener especial cuidado en los productos que se extraen de la planta, ya que algunas pueden tener compuestos alérgenos o irritantes, o estar contaminadas con microorganismos patógenos que pueden contaminar el producto y suponer un riesgo para la salud de los trabajadores y de los consumidores.
restos de disolvente
Uno de los puntos en la calidad de un fármaco que más preocupan son los restos de disolventes que pueden quedar en él. No siempre es posible sustituir los disolventes usados por otros inocuos o incluso llegar a eliminarlos por completo, por lo que existe una estricta regulación al respecto. La Conferencia internacional sobre armonización de los requisitos técnicos para el registro de productos farmacéuticos de uso humano (ICH) propuso una guía [27] en la que se clasifican los disolventes en cuatro grupos distintos:
- clase 1: Estos disolventes deben ser evitados a toda costa, a no ser que se imposible su reemplazo.
- clase 2: Los disolventes de esta clase deben ser reemplazados si es posible. Además existen límites en cuanto a concentración máxima y a ingesta diaria.
- clase 3: disolventes menos tóxicos y que pueden ser usados con limitaciones menos estrictas que los de la clase 2. Deben usarse estos cuando sea práctico.
- clase 4: Disolventes sin datos sobre su seguridad.
Conclusiones
La fabricación de fármacos es un proceso en el que el uso de disolventes es necesario para conseguir productos de alta necesidad en nuestra sociedad. Su presencia en el producto final no es deseable por sus efectos tóxicos o la degradación que puede suponer en el propio fármaco, por lo que se estudian e implementan soluciones para sustituir los disolventes por otros más seguros, o al menos, reducir su uso, cosa que no siempre es posible.
referencias
- ↑ Sheldon, Roger A., The E factor: fifteen years on, Green Chemistry, 2007
- ↑ Richard K. Henderson, Expanding GSK's solvent selection guide- embedding sustainability into solvent selection starting at medicinal chemistry, Green Chemistry, 2011, vol. 13, 854
- ↑ Antonio Tabernero, Supercritical fluids for pharmaceutical particle engineering: Methods, basic fundamentals and modelling, Chemical Engineering and Processing: Process Intensification, 60 (2012) 9-25
bibliografía
- Disolventes y métodos de reacción no convencionales. (Máster en Química Sostenible, año 2012-2013, Universidad de Zaragoza)
- enciclopedia de seguridad en el trabajo, capítulo 79, Industria farmaceútica
- ICH Q3C
- Katarzyna Grodowska and Andrzej Parczewski, Organic solvents in the pharmaceutical industry - review, Acta Poloniae Pharmaceutica n Drug Research, Vol. 67 No. 1 pp. 3n12, 2010
- guía de selección de GSK
Si bien es cierto que los disolventes facilitan el proceso químico (mezcla de reactivos, consecución de concentraciones adecuadas, control de la temperatura de reacción, etc), también lo es que presentan muchos inconvenientes, como un gran impacto tanto a nivel ambiental como para la salud de los seres humanos, riesgos de toxicidad, incendio o explosión, pérdidas por evaporación con sus consecuentes emisiones a la atmósfera, vertidos, uso en cantidades mucho mayores a las del producto, aumento de costes y riesgos de producción, requerimiento de una etapa de separación disolvente-producto final, o su origen, mayoritariamente fósil. Por ello, entre las exigencias medioambientales más importantes en el ámbito industrial, destaca la necesidad de sustituir el uso de disolventes, especialmente los clorados, por otros productos y/o procesos más sostenibles.
Sustitución de disolventes
El objetivo está marcado claramente, y no es otro que llevar a cabo la sustitución de disolventes siguiendo unos firmes criterios, como evitar o minimizar su uso, evitar los COV´s, utilizar disolventes menos tóxicos y fomentar el uso de disolventes renovables. La mejor forma de cumplir este objetivo es marcar y seguir una serie de pasos:
- Estudio del proceso.
- Evaluación de los riesgos.
- Indicación y evaluación de las alternativas.
- Comparación ¿Es realista la sustitución? ¿Cuáles son los costes? ¿Cuáles son las consecuencias?
- Efectuar la sustitución, con la participación y correcta formación de los trabajadores.
- Evaluación del cambio.
- Seguimiento.
A veces, esta sustitución puede ser una tarea muy complicada, sobre todo en el caso de los disolventes que actúan como medio de reacción, por su influencia en:
- Velocidad de reacción (cinética)
- Quimioselectividad
- Regioselectividad
- Estereoselectividad
- Rendimiento de reacción
Sin embargo, es una oportunidad para adoptar una nueva tecnología. Todas las grandes empresas han eliminado determinados disolventes (por ejemplo: tetracloruro de carbono, CCl4) e intentan evitar otros (por ejemplo: diclorometano o cloruro de metileno, CH2Cl2) a menos que sea imprescindible. El gran inconveniente es el alto precio pero a pesar de ello, la tendencia es clara, ya que se ha producido una disminución significativa en el uso de hidrocarburos y clorados y un aumento en el de alcoholes y derivados.
A modo de ejemplo: se calcula que los procesos industriales de Europa occidental emplean entre 50.000 y 100.000 sustancias químicas diferentes. Sin embargo, unas 1.000 de estas sustancias constituyen el 90% del total. Una de las más importantes es el tricloroetileno (TCE), un disolvente utilizado en la industria para limpiar y desengrasar. En Suecia, la sustitución o reemplazamiento de las sustancias peligrosas por otras más seguras es un concepto fundamental. El uso comercial del TCE se prohibió en 1991 de acuerdo con una petición del sindicato de la metalurgia para que se fuera eliminando poco a poco. Se concedieron cinco años a la industria para adaptarse. El uso del TCE se redujo significativamente, desde 6.000 toneladas en 1987 a 700 en 1997. Las empresas que decidieron posponer el cambio ahorraron dinero a corto plazo pero las que tenían una visión del futuro aprovecharon la oportunidad para sustituir la maquinaria ineficaz. Además, se dieron cuenta de que serían más competitivas a largo plazo, cuando otros países de la UE empezaran a eliminar paulatinamente el TCE. En otra campaña de sustitución, los dividendos económicos fueron más inmediatos, ya que al sustituir los productos de limpieza y tintas a base de disolvente por otros de base vegetal, los procesos de impresión utilizaron la energía de forma más eficaz, lo que redujo considerablemente los costes de producción.
Riesgos para el medio ambiente
El uso de disolventes libera a la atmósfera compuestos orgánicos volátiles (COV´s), que provocan problemas importantes en el entorno natural, como la degradación y destrucción de la capa de ozono (agujero de la capa de ozono), como es el caso de 1,1,1-tricloroetano, el tetracloruro de carbono, los CFC´s o los HCFC´s. De forma general también contribuyen a la formación de ozono ambiental o troposférico (es decir, en las capas bajas de la atmósfera) en presencia de la luz solar, causando efectos nocivos tanto para la salud humana (provoca afecciones en la capacidad respiratoria) como para el medio ambiente (interfiere en el crecimiento de la vegetación y cultivos, aumenta su sensibilidad a plagas, seguías y heladas, y producce smog).

La legislación establece límites de protección, y considera a los disolventes orgánicos así como a sus envases vacíos, trapos o cualquier otro material que se haya utilizado para su aplicación, residuos peligrosos. Por lo tanto, deben ser gestionados por un gestor autorizado.
Riesgos para la salud
El carácter volátil de los disolventes hace que éstos se evaporen rápidamente en el aire, alcanzando concentraciones importantes en espacios confinados. Los riesgos mayores para el ser humano se producen por la absorción de éstos a través de la piel y por inhalación.
El contacto directo con la piel permite su absorción, y que el disolvente pase a la sangre, causando efectos inmediatos y a largo plazo. Algunos disolventes orgánicos como los clorados, son liposolubles, es decir, que una vez que se introducen en el organismo tienen afinidad por los tejidos grasos. Con el paso del tiempo las concentraciones acumuladas pueden alcanzar niveles que representen un riesgo para la persona y, en particular, para un feto si asimila esta contaminación a través de su madre durante su desarrollo embrionario y el período de lactancia.
Por ello, algunos disolventes están asociados a la irritación ocular, molestias nasales y de garganta, jaquecas, reacciones cutáneas y alérgicas, disnea, nauseas, fatiga, mareo, aborto espontáneo, malformaciones congénitas, lesiones cerebrales, interferencias en la capacidad reproductiva, o al cáncer infantil.
En algunos estudios de toxicidad, en los que se relacionan las lesiones neurológicas con la exposición crónica a disolventes, los investigadores hallaron un menor rendimiento en los trabajadores/as que estaban expuestos a niveles inferiores a los máximos legales fijados por las autoridades.
Además, la mayoría de los disolventes son inflamables y explosivos, lo que representa otro tipo de riesgo diferente asociado a estas sustancias. Algunos no arden necesariamente con facilidad, pero sí tienden a descomponerse a altas temperaturas dando lugar a otros compuestos altamente tóxicos. Este es el caso de los disolventes halogenados, que se convierten en fosgeno, ácido clorhídrico, ácido fluorhídrico, etc.
Buenas prácticas
La línea prioritaria de intervención en la industria frente a este problema viene definida en la Ley de prevención de riesgos laborales: eliminación del riesgo. La prevención, por tanto, en el caso de la utilización de disolventes se lograría mediante la sustitución de materias primas, procesos o productos. Hasta que se logre eliminar o reducir los riesgos, siempre se deben incorporar mejoras en los hábitos y en la organización del trabajo que permitan reducir aquellos que sean innecesarios. Estos cambios o hábitos son las llamadas buenas prácticas. Algunos ejemplos son:
- Evitar la necesidad de uso de disolventes.
- Elegir los disolventes que sean menos peligrosos.
- Maximizar la eficacia de la operación.
- Estandarizar el uso de los disolventes.
- Extraer frecuentemente los fangos o residuos de los tanques de disolventes.
- Aumentar el grado de agitación en los baños.
- Controlar las pérdidas por evaporación.
- Reducir la velocidad de extracción y permitir un amplio tiempo de drenaje.
- Mantener los disolventes segregados con el fin de optimizar su reciclaje y/o tratamiento.
- Mantener los residuos de disolventes lo menos contaminados posible para facilitar su reciclaje.
Los riesgos para la salud y el medio ambiente son grandes pero sin embargo, cambiar la política exige decisiones difíciles. Actualmente, dependemos de un número cada vez mayor de esta clase de productos químicos, con los que se ha reducido el coste financiero de la producción en serie y se ha contribuido a garantizar una mayor distribución material. Aplicar el principio de precaución y eliminar escalonadamente las sustancias peligrosas puede desembocar en la pérdida o aumento de puestos de trabajo, según la situación, por lo que una buena planificación resulta esencial para encontrar el justo equilibrio entre beneficios y costes, esencial en la industria. Lo importante es combinar los beneficios con el desarrollo de sustancias y procesos químicos más seguros.
Motivos para el uso de disolventes "verdes"
- Aplicación y desarrollo de nuevas rutas sínteticas de bajo impacto ambiental.
- Sustitución de disolventes para eliminar las emisiones de compuestos orgánicos volátiles (COV´s), toxicidad e inflamabilidad.
- Uso de materias primas renovables.
- Uso de reactivos seguros para reducir el impacto sobre la naturaleza (inocuos para el medio ambiente) y la exposición humana a productos químicos peligrosos.
- Uso de nuevas tecnologías más sostenibles.
- El uso de estas técnicas permiten eliminar o reducir:
- El uso de productos tóxicos persistentes en síntesis química.
- El número de etapas sintéticas y aislamientos para economizar los procesos de producción.
- El número de toneladas de residuo por producto comercializado.
- El uso o generación de solventes y sustancias nocivas y tóxicas en los procesos de síntesis y producción.

Los disolventes verdes deben ser, ante todo, fácilmente separables de los productos y reutilizables
Entre las aplicaciones de los disolventes "verdes", destaca su empleo como pesticida debido a las siguientes ventajas:
- Aumentan la eficiencia del pesticida.
- Poseen baja resistencia.
- Aumentan selectividad.
- Gran poder de solvencia.
- Son biodegradables.
- Reducen la contaminación.
- Baja toxicidad para animales sangre caliente.
- No tóxico para peces, gusanos, daphnia.
- Alto Flash Point.
Otras aplicaciones de esta familia de disolventes son, por ejemplo:
- Revestimientos: Pinturas, adhesivos (el solvente es usualmente extraído por evaporación después su aplicación)
- Limpieza: Limpiadores secos
- Extracción: Aceites, descafeinización del café (benceno, CH2Cl2)
- Farmacia: Producción de principios activos.
- Producción de biocombustibles: Biodiésel y subproductos
Disolventes alternativos
¿Cuál es el disolvente mas "verde"? Ninguno lo es completamente, ya que depende de la aplicación a la que se destine. El problema no es tanto su empleo como las ineficiencias inherentes asociadas con su contención, recuperación y reutilización. Los disolventes verdes deben ser, ante todo, fácilmente separables de los productos y reutilizables, y consecuentemente, para evaluar el verdor es necesario considerar todo su ciclo de vida. A continuación se presentan varias alternativas.
Disolventes reactivos
Forman una familia de disolventes que tienen una baja volatilidad relativa y la capacidad de reaccionar con otros componentes, evaporándose al medio ambiente. Una característica importante es que no constituyen COV´s.
Disolventes benignos
Se trata de disolventes que no dañan el medio ambiente. En este grupo se encuentran los disolventes libres de compuestos clorados, los cuales tienen una baja toxicidad si son comparados con los convencionales.
Disolventes neotéricos
El término neo significa nuevo, reciente, contemporáneo, moderno, e involucra a disolventes que muestran una menor toxicidad, son más seguros y menos contaminantes que los disolventes convencionales. Entre ellos se incluyen tanto nuevos fluídos con propiedades ajustables, como compuestos que no son o son poco usados en la actualidad como disolventes, pero que tienen un gran potencial de uso futuro en este campo porque permitirían adoptar un mayor grado de sostenibilidad en futuras aplicaciones.
Disolventes neotéricos
Los disolventes neotéricos se pueden obtener a partir de materias primas renovables, siendo una muy buena alternativa a los disolventes derivados del petróleo. Un ejemplo de ellos son los procedentes de la biomasa. La mayoría de estos disolventes presentan una baja toxicidad y volatilidad, no son corrosivos ni cancerígenos, y además muchos de ellos se obtienen a partir de residuos vegetales, lo que les hace económicamente competitivos.
Química sin disolventes
“El mejor disolvente es ningún disolvente” (The best solvent is no solvent). Ciertamente, es una opción que se presenta como ideal bajo muchos aspectos, como el económico o el de la sencillez. De hecho, un gran número de productos se obtienen en procesos que no emplean disolvente, pero la novedad consiste en tratar de ampliar las posibilidades de realización de reacciones y procesos químicos que hasta ahora se habían considerado irrealizables en ausencia de disolventes.
No todas las reacciones son posibles, pero con mayor o menor dificultad (a veces es necesario el uso de catalizadores y/o soportes), pueden llevarse a cabo reacciones de todo tipo: Sólido-Sólido, Sólido-Líquido, Sólido-Gas, Líquido-Líquido, Líquido-Gas, Gas-Gas.
Las ventajas y desventajas de la química sin disolvente son:

Ventajas:
- Los reactantes presentan una concentración máxima. (mayor reactividad)
- Menor consumo energético, al no tener que calentar la masa de disolvente.
- Activación por microondas más simple.
- Menor volumen de reactor para el mismo volumen de producción. (mayor productividad en el mismo volumen de reactor)
- Proceso más simple y económico.
Desventajas:
- Menor dinamismo molecular.
- En algunos casos, dificultades para la mezcla eficiente, especialmente con reactivos o productos sólidos.
- Dificultad para el manejo de líquidos viscosos.
- Las reacciones exotérmicas pueden ser peligrosas en su aplicación a gran escala.
- No aplicable a muchas reacciones.
La realización de una reacción sin disolvente no necesariamente obvia el empleo de disolventes en las fases de separación y purificación del producto, pero en cualquier caso da ocasión a la reducción del volumen empleado.
Agua
En el siglo XIX, la mayor parte de las síntesis químicas se llevaban a cabo en agua. Más tarde, el auge de la Química Orgánica en el siglo XX, con compuestos que presentan baja solubilidad en ella, la relegó a un papel minoritario como disolvente.

Sin embargo, el agua siempre ha sido denominado como el disolvente universal porque es la mejor elección en caso de que exista una demanda de uso de disolvente, ya que no es inflamable ni tóxica, y es respetuosa con el medio ambiente. Por contra, presenta el inconveniente de que las reacciones en condiciones homogéneas tienen poco interés industrial debido a la baja velocidad de reacción y solubilidad de los reactivos, la necesidad de extracción de los productos con un disolvente orgánico, y que su bien ordenada estructura hace que calentarla/evaporarla o enfriarla (para lo cuál hay que romper puentes de hidrógeno) suponga un alto coste energético.
El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno (cada molécula de agua puede ceder y aceptar dos puentes de hidrógeno con las moléculas vecinas) hacen que el agua sea un excelente disolvente. De este modo, una molécula o ion es soluble en agua si puede interactuar con las moléculas de la misma mediante puentes de hidrógeno o interacciones del tipo ion-dipolo.
Conforme aumenta la temperatura y la presión, las propiedades del agua varían. Por ejemplo, la constante dieléctrica disminuye y se hace más similar a la de los disolventes orgánicos, pudiendo llegar a disolver algunos de estos compuestos mediante un proceso en fase homogénea, hecho que facilita la separación del soluto por enfriamiento y la eliminación de residuos.
Resumen de propiedades del agua:
- Barata, fácilmente disponible y abundante.
- No tóxica, no inflamble, no COV y de manejo seguro.
- Mal disolvente de compuestos apolares: inapropiada para reacciones orgánicas homogéneas, útil en procesos bifásicos junto a otros disolventes, fácil separación de la mayoría de compuestos orgánicos.
- Uso de grandes volúmenes.
- Incompatible con muchos reactivos.
- Altos costes energéticos.
Algunas de las reacciones interesantes con agua son: Reacciones no catalizadas (Diels-Alder, Claisen, condensación, polimerización radicalaria), reacciones catalizadas (por ácidos de Lewis, reactivos organometálicos, condensación aldólica), reacciones con agua subcrítica, supercrítica, sistemas bifásicos, hidrogenación, hidroformilación, carbonilación, hidroxicarbonilación, hidroxicianación, reacciones de acoplamiento, y catálisis micelar.
Disolventes orgánicos renovables

La aproximación más simple para la superación de los inconvenientes de los disolventes empleados actualmente por las industrias y sectores que utilizan disolventes orgánicos, consiste en su sustitución por nuevos disolventes orgánicos, ya que con frecuencia su uso resulta inevitable o presenta ventajas difíciles de superar (mayor solubilidad de los solutos, facilidad de separación). La necesidad de superación de las fuentes fósiles lleva a la necesidad de la preparación de nuevos disolventes a partir de la biomasa, y motiva una nueva línea activa de innovación e investigación acerca de las fuentes de materias primas renovables.
Su origen, por tanto, es sostenible, son biodegradables, tienen un gran poder para disolver un amplio abanico de sustancias, presenta una baja o nula toxicidad, no son corrosivos, carcinógenos, ni destruyen la capa de ozono.
Por contra, son más caros que los disolventes convencionales, aunque los costes disminuirían y se volverían competitivos al aumentar el mercado y los avances tecnológicos. Además, pueden ser inflamables y presentan una alta volatilidad, lo que puede generar COV´s.
Este tipo de disolventes son producidos a grandes cantidades en biorefinerías y lo componen una amplia variedad de compuestos, como hidrocarburos, ácidos, alcoholes, éteres, o ésteres. Algunos ejemplos interesantes son: Limoneno, Metanol, Etanol, Glicerol, 2-Metiltetrahidrofurano, Lactato de etilo, Lactato de 2-etilhexilo, Biodiésel, Laurato de isopropilo, Triacetina.
Fluidos supercríticos
Un fluido supercrítico (FSC o SCF: supercritical fluid, en inglés) es toda sustancia que se encuentra por encima de su punto crítico, es decir, que cuyas condiciones se encuentran por encima de su temperatura crítica (Tc) y presión crítica (Pc). Presentan propiedades intermedias entre gas y líquido, poseyendo el poder disolvente de los líquidos y la difusividad de los gases, por lo que podrían ser considerados como "gases densos".
Tienen un gran papel en la química sostenible por su importancia como disolvente alternativo porque suponen una reducción globalmente muy importante del uso de disolventes orgánicos, son inertes y no tóxicos, su coste es relativamente barato y se pueden variar sus propiedades mediante variaciones de presión. La propiedad más característica de los fluidos supercríticos es el amplio rango de altas densidades que pueden adoptar dependiendo de las condiciones de presión o de temperatura, a diferencia de los líquidos, que son prácticamente incompresibles, y de los gases, que poseen densidades siempre muy bajas.

Algunas de las ventajas que ofrecen los FSC son:
- Mejor transporte.
- Totalmente miscibles con gases.
- Nula tensión superficial y viscosidad.
- Medioambientalmente benignos.
- Propiedades ajustables mediante P.
- Excelentes para procesos de extracción.
- Inertes.
- No tóxicos.
- Relativamente baratos, pero requieren equipos complejos y costosos.
- Disolventes ”verdes”.
Existe una amplia variedad de FSC y su elección en cada caso depende de cuál vaya a ser su uso. Los más utilizados son el agua supercrítica (scH2O: Tc= 374.2 ºC, Pc= 220.5 bar) y el dióxido de carbono supercrítico (scCO2: Tc= 31.1 ºC, Pc= 73.8 bar) ya que tienen unas condiciones, sobretodo el scCO2, fácilmente accesibles.
| Solvente | Peso molecular | Tº crítica | Presión crítica | Densidad crítica |
|---|---|---|---|---|
| g/mol | K | MPa (atm) | g/cm3 | |
| Dióxido de carbono (CO2) | 44,01 | 304,1 | 7,38 (72,8) | 0,469 |
| Agua (H2O) | 18,02 | 647,3 | 22,12 (218,3) | 0,348 |
| Metano (CH4) | 16,04 | 190,4 | 4,60 (45,4) | 0,162 |
| Etano (C2H6) | 30,07 | 305,3 | 4,87 (48,1) | 0,203 |
| Propano (C3H8) | 44,09 | 369,8 | 4,25 (41,9) | 0,217 |
| Etileno (C2H4) | 28,05 | 282,4 | 5,04 (49,7) | 0,215 |
| Propileno (C3H6) | 42,08 | 364,9 | 4,60 (45,4) | 0,232 |
| Metanol (CH3OH) | 32,04 | 512,6 | 8,09 (79,8) | 0,272 |
| Etanol (C2H5OH) | 46,07 | 513,9 | 6,14 (60,6) | 0,276 |
| Acetona (C3H6O) | 58,08 | 508,1 | 4,70 (46,4) | 0,278 |
A priori, los FSC ofrecen una gran cantidad de ventajas, aunque la realidad industrial es que en toda Europa hasta el 2005 había menos de 40 instalaciones con estas tecnologías y en estos momentos su número ha aumentado, pero no significativamente. Esto de debe a que para introducir una tecnología nueva, los costes son casi prohibitivos e impiden que se puedan implementar. Además, el 40% del coste es la amortización de los equipos y esto hace que las empresas sean muy prudentes, aunque a pesar de esto existen y cada vez su desarrollo y utilización va a más.
Líquidos iónicos
Los líquidos iónicos (ionic liquids, en inglés) son sales de un catión orgánico y un anión inorgánico cuyo punto de fusión es inferior a 100 ºC y que resultan líquidas dentro de un amplio margen de temperaturas. Al ser iónicos, presentan una presión de vapor muy baja, hasta poder ser considerados como no volátiles. Su estabilidad térmica puede ser muy elevada y alcanzar temperaturas de hasta 300 ºC sin sufrir ninguna alteración.
Los cationes orgánicos más frecuentes son los iones imidazolio, piridinio y los amonio y fosfonio cuaternarios. Por lo que respecta a los aniones, son frecuentes los tetrafluoroboratos (BF4), hexafluorofosfatos (PF6), y los tetracloroaluminatos (AlCl4), pero también se suelen utilizar iones cloruro, bromuro o nitrato, entre otros.

El número de líquidos iónicos producidos comercialmente es relativamente reducido frente a las enormes posibilidades de combinación de cationes y aniones fácilmente asequibles. Su fácil preparación permite el diseño del disolvente más adecuado para un proceso concreto, y lograr modificaciones en el punto de fusión, viscosidad, acidez o basicidad. Su densidad varía en función de la cadena y el anión aunque son siempre más densos que el agua, y su miscibilidad en ella depende de la naturaleza del anión y catión que lo formen. Por otra parte, su viscosidad aumenta con la longitud de la cadena (aumento de las interacciones de Van der Waals) y disminuye con las ramificaciones.
Esta familia de disolventes puede presentar notables ventajas frente a los convencionales para las reacciones de síntesis. Son comparables, con ventaja en muchas ocasiones, con los disolventes polares apróticos, mientras que su inmiscibilidad con agua y disolventes orgánicos y su estabilidad térmica pueden ser utilizadas para la separación del producto, aunque no de manera simple. Otra ventaja que presentan es su alto grado de reutilización, circunstancia que puede compensar los aspectos contaminantes de su preparación. Además, pueden actuar como catalizador e introducir quiralidad en su estructura. Sin embargo, no todo son ventajas, ya que los líquidos iónicos habituales tienen una difícil purificación, baja inflamabilidad (dificulta la incineración), propiedades corrosivas y muestran una biodegradabilidad muy baja y cierta neurotoxicidad. En cuanto a su accesibilidad, por lo general son muy caros pero el precio varía mucho en función del procedimiento se síntesis que se haya llevado a cabo (por lo general, síntesis complejas y poco sostenibles) y de los iones que lo compongan. Por ejemplo, los cationes más caros y baratos son el [dialquilimidazolio]+ y el [HNR3]+, respectivamente, mientras que los aniones son el [SbF6]- y el [Cl]-.
Las propiedades y posibilidades de su empleo en procesos industriales es de indudable interés y ha llevado ya a su utilización industrial. El estudio se dirige a aspectos quimicofísicos, reacciones clásicas, sistemas catalíticos y biocatalíticos, y a aplicaciones que no implican reacción química, aunque en la actualidad se ha ampliado al campo de los lubricantes y fluídos de transferencia térmica, extracción de sustancias volátiles resultantes en procesos fermentativos, producción de gasolinas y en electroquímica.
Disolventes perfluorados
Los llamados disolventes fluorados bifásicos (fluorous biphasic solvent) suelen ser perfluoroalcanos, perfluorodialquiléteres o perfluorotrialquilaminas de cadena lineal o ramificada de entre 6 y 10 átomos de carbono en los que todos los átomos de hidrógeno han sido sustituídos por flúor (enlace C-H sustituído por enlace C-F muy fuerte). Se habla también de disolventes fluorosos (término introducido por István T. Horváth en 1994) por analogía con los medios acuosos. Para indicar un compuesto perfluorado ha sido aceptado por la IUPAC el empleo del prefijo F. Por ejemplo, F-ciclohexano por perfluorociclohexano o F-trihexilamina por perfluorotrihexilamina.

Puede decirse que son simultáneamente hidrófobos y lipófobos aunque la miscibilidad es fuertemente dependiente de la temperatura, y aquí es donde se basa en gran medida su utilidad. Son inmiscibles con muchos disolventes orgánicos (THF, tolueno, acetona) y con el agua, lo que facilita el uso de sistemas bifásicos y la separación de productos. Como características, se puede destacar que son químicamente inertes, por lo que se evitan reacciones laterales que presentan algunos de los disolventes orgánicos comunes. Son térmicamente estables, por lo que se pueden emplear sin peligro a altas temperaturas. No son inflamables ni tóxicos, por lo que se minimizan los riesgos asociados a su aplicación industrial. Poseen un amplio intervalo de puntos de ebullición (de 50ºC a 220ºC), pueden destilarse y reutilizarse, y son más densos que el agua y los disolventes orgánicos. Respecto a las propiedades asociadas a su estructura, se puede destacar que el átomo de flúor es muy electronegativo y muy poco susceptible a la polarización. La baja polarizabilidad hace que las fuerzas de Van der Waals sean inferiores a las de los hidrocarburos correspondientes y en consecuencia su volatilidad sea superior.
Como aspectos negativos de estos disolventes polifluorados cabe descatar su elevado coste y la falta de datos acerca de sus efectos ambientales en la Biosfera, porque a pesar de que se presenten como no tóxicos, existe cierta preocupación sobre su volatilidad, persistencia e impacto ambiental. De manera similar a los líquidos iónicos, se puede decir que los disolventes perfluorados presentan un indudable interés para reducir el volumen de disolventes orgánicos convencionales empleados, pero existen serias dudas acerca de su inocuidad ambiental y sus efectos.
Las reacciones más comunes asociadas a estos disolventes son: oxidación, epoxidación, hidroformilación, polimerización radicalaria y reacciones biocatálizadas.
Polímeros líquidos

Los polímeros líquidos presentan un orden intermedio, combinando las propiedades de los sólidos cristalinos (anisotropía) con la de los líquidos (flujo). Los más utilizados son principalmente el PEG (polietilenglicol), y también el PPG (polipropilenglicol), PTHF (politetrahidrofurano), y el PMPS (polimetil-fenilsiloxano).
En cuanto sus propiedades, tienen un amplio intervalo de pesos moleculares, pueden usarse tanto en sistema homogéneos como heterogéneos, no son volátiles ni tóxicos, se pueden reciclar, son muy estables y baratos, pueden formar complejos para usarse en catálisis de fase, y poseen un amplio catálogo de características distintas (viscosidad, resistencia, peso molecular, etc) en función de cuál se utilice.
Las principales aplicaciones se encuentran en reacciones de Diels-Adler, acoplamiento de Heck, sustitución nucleófila, oxidación, dihidroxilación, reducción, catálisis de trasferencia de fase (PTC) y extracción de productos naturales a partir de biomasa.
Perspectiva
El carácter fluido y con frecuencia volátil de los disolventes, junto a su facilidad para inflamarse, a dar mezclas explosivas con el aire, o su toxicidad, hace que el empleo de disolventes orgánicos constituya una de las fuentes más importantes de peligro en la industria química. A ello se une la fácil dispersión, la persistencia y la ecotoxicidad en el ambiente de los disolventes clorados. El origen fósil y el volumen con que se emplean los disolventes orgánicos en las fases de reacción y de aislamiento y purificación de los productos potencian enormemente la contribución del proceso industrial a la contaminación ambiental.
Los estudios y ensayos para la sustitución de los disolventes orgánicos clásicos por otros de origen renovable, está en la actualidad en una fase de enorme actividad dentro de la Química Sostenible. Una de las virtudes de esta reacción ante los problemas que plantean los disolventes ha sido promover la dedicación generalizada al estudio de los fundamentos quimicofísicos de la función del disolvente. Este estudio viene acompañado de la inventiva para conseguir nuevos disolventes , algunos tan asequibles como el agua o la ausencia de disolvente, otros aprovechando fases poco exploradas como las supercríticas, y otros de diseño totalmente nuevo como los líquidos iónicos o los disolventes perfluorados. Se busca, de esta forma, poder diseñar el disolvente más limpio e idóneo para el procesos específico que se pretende realizar.
De todo este movimiento científico-tecnológico que gira alrededor de los disolventes, las aplicaciones que más fácilmente penetran en la práctica de la industria son aquellas que no requieren cambios notorios en la rutina establecida de los procesos habituales, permiten el empleo de los mismos reactores y sistemas de control, mejoran los rendimientos, facilitan la seguridad, reducen la generación de residuos, y que resultan económicamente beneficiosas. La introducción de los disolventes neotéricos es más lenta, al requerir cambios mucho mayores, no resultar siempre rentables económicamente, y algunos de ellos, como los líquidos iónicos y los disolventes fluorosos, al no quedar bien definida su inocuidad para las personas y el medio ambiente.
Conclusiones
La Unión Europea estima que en la Comunidad se emiten cada año alrededor de 10 millones de toneladas de compuestos orgánicos volátiles procedentes de los carburantes y disolventes. En marzo de 1999 se aprobó la Directiva 99/13 relativa a la “limitación de las emisiones de compuestos orgánicos volátiles debidas al uso de disolventes orgánicos en determinadas actividades e instalaciones”. En esta directiva se prevé reducir en dos tercios el uso de compuestos orgánicos volátiles liberados en la atmósfera por el uso de disolventes industriales, y la mejor forma de reducir este uso es llevar a cabo la sustitución de disolventes convencionales por disolventes neotéricos, aumentando su estudio, empleo y aplicación.
Referencias
Bibliografía
- Disolventes y métodos de reacción no convencionales. (Máster en Química Sostenible, año 2012-2013, Universidad de Zaragoza)
- Fundamentos de la Sostenibilidad y de la Química Sostenible. (Máster en Química Sostenible, año 2012-2013, Universidad de Zaragoza)
- Ramón Mestres: "Química Sostenible". Ed. Síntesis, Madrid (2011)
- Estefanía Blount: "Estrategias de sustitución y estrategias de control. Estudio de casos prácticos", El Escorial (2001)