Disolventes en la Industria Química/Impacto ambiental de los disolventes
Debido a las prácticas industriales, la utilización de los disolventes ha generado una buena modificación de la reactividad, disolución de sustancias, eficaz transporte de masa y energía, entre otros. Pero que a su vez presentan riesgos para la salud de los seres vivos y la preservación del medio ambiente, ya que el problema con los disolventes no es tanto su empleo como lo mal asociado con su contención, recuperación y reutilización.
En la actualidad, han aumentado las consideraciones ambientales ocupando un lugar cada vez más importante en la industria química, saciando el deseo de los consumidores preocupados y los fabricantes para elegir los productos más respetuosos para el medio ambiente; este ha llevado al desarrollo de la evaluación del ciclo de vida (LCA) y el diseño para el medio ambiente (DfE). Evitando o eliminando grandes cantidades de emisiones provenientes del uso desmedido de los disolventes en la industria.
Peligros para la salud
[editar]Todos los beneficios que mejoran la calidad de vida, resultan innegables las diversas formas de contaminación y los incidentes graves en forma de explosión, incendios, intoxicaciones masivas, pueden ser causa de incidentes personales o públicos altamente dramáticos que tienen con gran frecuencia origen en el uso de los disolventes en la actividad química industrial.
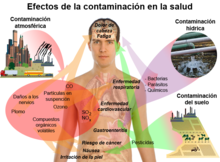
El carácter volátil de los disolventes hace que éstos se evaporen rápidamente en el aire, alcanzando concentraciones importantes en espacios confinados. Los riesgos mayores para el ser humano se producen por la absorción de éstos a través de la piel y por inhalación. El contacto directo con la piel permite que el disolvente pase a la sangre, causando efectos inmediatos y a más largo plazo. La inhalación constituye la vía de exposición más peligrosa, porque los pulmones son muy eficaces en distribuir éstas, o cualquier otra sustancia, por todo el cuerpo pudiéndose inhalar concentraciones muy elevadas en plazo breve, siendo esta vía, además, particularmente difícil de controlar. [1]
Los efectos sobre la salud pueden variar según el compuesto, estos dependerán de la naturaleza de cada compuesto y del grado y del periodo de exposición al mismo. Según el 10º Informe sobre Carcinógenos, se sabe que el benceno es un carcinógeno humano y se presume razonablemente que el formaldehído y el percloroetileno son carcinógenos. Las personas con mayor riesgo de exposición a largo plazo a esos tres compuestos orgánicos volátiles son los trabajadores industriales que tienen una exposición ocupacional prolongada a los compuestos, los fumadores y las personas expuestas por períodos prolongados a las emisiones del tránsito pesado de vehículos automotores.
Exposición e Intoxicación
[editar]El mayor campo de contacto, es en las industrias donde el trabajador expuesto al disolvente, como consecuencia de esa exposición, puede desarrollar un daño en su organismo. Ese daño será proporcional a una serie de factores como son:
- Los propios de la naturaleza humana.
- Los característicos de los disolventes (su toxicidad).
- La velocidad de absorción por el organismo.
- La concentración en el ambiente.
- Tiempo de exposición.
Para que un trabajador se vea afectado por un tóxico,no dependerá sólo de la dosis recibida, sino también de la forma y el tiempo que tarde en administrarse esa dosis. Hay 3 tipos de intoxicaciones según su velocidad de penetración en el organismo: aguda, subaguda y crónica. [2]
Prevención
[editar]Son aquellas medidas cuyo objeto es impedir que los riesgos a los que está expuesta la trabajador den lugar a situaciones de emergencia.
Las acciones de prevención las aplicamos:
- Foco contaminante.
- Medios de propagación.
- El individuo.
Foco contaminante
[editar]Sustituir un disolvente por uno de menor toxicidad. Ejemplo: el tricloroetileno por el 1,1,1 tricloroetano
Medios de propagación
[editar]Generar una ventilación localizada, realizar la limpieza por procedimientos húmedos o aspirado (equipos que pierden disolventes, en contacto con la atmósfera, se evaporan y se mezclan con el aire) y sistemas de alarmas para el aumento desproporcional de concentraciones en el foco contaminante.
Individuo
[editar]Sobre el individuo puede actuarse en su buen uso de la higiene y protección personal, la formación e información sobre el disolvente a tratar en el trabajo diario. Como también hacer rotaciones, para disminuir la exposición del trabajador.
Alternativas
[editar]Existen sistemas de limpieza de piezas que eliminarían la necesidad de utilizar disolventes, y que ofrecen mejores resultados que los procesos tradicionales:
- Limpieza acuosa automatizada.
- Lavado acuoso con potencia.
- Limpieza ultrasónica.
- Flujos bajos en sólidos.
- Soldadura en atmósfera inerte.
Existen otras experiencias prácticas, que demuestran la existencia de numerosas tecnologías que son más respetuosas con la salud de trabajadores/as y el medio ambiente y la viabilidad económica de las mismas. Un ejemplo es el caso de una empresa mediana en EE.UU, fabricante de herramientas, que sustituyó su sistema de desengrase de las piezas basado en tricloetileno por un agente no tóxico y biodegradable, el d‐limoneno, que es una sustancia química natural que se extrae a partir de la esencia de cítricos principalmente.
Ademas de calcular:
- Valores umbral límites (TLV): concentración a la que la mayoría de los trabajadores puede exponerse sin riesgos durante un período de 8 horas.
- Concentraciones máximas autorizadas (CMA): para los venenos aerotransportados. [3]
Peligros para el medio ambiente
[editar]Los productos químicos causantes de la contaminación del ambiente son también nocivos y peligrosos, pero a través de efectos que se manifiestan de manera no inmediata y que ademas permanecen durante periodos prolongados de tiempo.
La industria química suele emplear sustancia químicas en cantidades elevadas, con riesgo de vertidos ocasionales o de emisiones mejor o peor controladas. En la siguiente tabla, se muestra los datos de sustancias toxicas emitidas por la Industia quimica de Estados Unidos, según datos de la Environmental Protection Agency de Estados Unidos (EPA). [4]
| Producto | Emisiones | Producto | Emisiones |
|---|---|---|---|
| Ácido clorhídrico | 657 | Ácido clorhídrico | 65 |
| Hidróxido sódico | 627 | n-Hexano | 72 |
| Metanol | 420 | Metanol | 241 |
| Tolueno | 345 | Tolueno | 127 |
| Acetona | 235 | Metiletilacetona | 60 |
| 1,1,1-Tricloroetano | 182 | Ácido fosforico | 63 |
| Diclorometano | 152 | Diclorometano | 54 |
| TOTAL | 2618 | TOTAL | 682 |
Los efectos nocivos de los productos emitidos al ambiente dependen naturalmente de su toxicidad, pero también de su persistencia y su movilidad en el ambiente. La vida media de los disolventes en medioambiente es alta.
Compuestos Orgánicos Volátiles (COV)
[editar]El uso de disolventes orgánicos suponen el 30%, del que aproximadamente el 20% representa el uso de disolventes en la industria. La evaporación de los disolventes orgánicos a partir de su uso en la industria, como ya se ha dicho, contribuye en una parte muy importante a estas emisiones. Basta indicar que entre los sectores de producción y aplicación de pinturas, el de impresión y las actividades de desengrase y limpieza de metales se produce el 65% de las emisiones.
Las emisiones de COV representan millones de toneladas anuales (directivas 99/13/CE, programa CAFÉ, REACH). [5]
Provocando consecuencia a su exposición:
A CORTO PLAZO
- Irritación ocular.
- Molestias nasales y de garganta.
- Jaquecas.
- Reacciones cutáneas alérgicas.
- Disnea.
- Naúseas.
- Fatiga.
- Mareo.
A LARGO PLAZO
- Lesiones del hígado.
- Los riñones.
- El sistema nervioso central. [6]

La emisión de compuestos orgánicos volátiles (COVs) a la atmósfera tiene algunos problemas importantes para el medio ambiente. Algunos COVs contribuyen a la degradación de la capa de ozono atmosférico, como es el caso del 1,1,1‐tricloroetano y el tetracloruro de carbono, así como de los CFCs y los HCFCs, entre otros.
Por otro lado, los COVs junto con los NOx en presencia de luz solar actúan como precursores de la formación de ozono troposférico y smog fotoquímico (Limitación de niveles, Directiva 92/72/CEE). Causando efectos nocivos para las especies vegetales y los cultivos, interfiriendo en las actividades fotosintéticas, en el crecimiento y en el metabolismo general, aumentando la sensibilidad de los árboles a las heladas, al calor y a la sequía.
Smog Fotoquímico
[editar]Contribuyen a la formación del smog fotoquímico al reaccionar con otros contaminantes atmosféricos (como óxidos de nitrógeno y con la luz solar, formando oxidantes fotoquímicos troposféricos (como formaldehído, monóxido de carbono e hidroperoximetilo. Este smog fotoquímico se da principalmente en áreas urbanas, dando lugar a atmósferas ricas en ozono de un color marrón.
La formación y destrucción de ozono:
Durante el día el dióxido de nitrógeno se disocia en monóxido de nitrógeno y radicales oxígeno:

:NO2 + hν → NO + O·
El O se combina con oxígeno molecular generando ozono:
:O· + O2 → O3
En ausencia de COVs este ozono oxida al monóxido de nitrógeno de la etapa anterior:
:O3 + NO → O2 + NO2
Pero en presencia de COVs, éstos se transforman en radicales peroxi que a su vez oxidan al NO:
:ROO· + NO → RO· + NO2
De esta forma el NO no está disponible para reaccionar con el ozono y el OZONO se acumula en la atmósfera. Muchos de los radicales RO· generados terminan formando aldehídos. Éstos, cuando la concentración de NO es baja (conforme avanza el día), pueden reaccionar con NO2 dando lugar a compuestos del tipo RCOOONO2 (cuando R es un metilo se denomina peróxido de acetilnitrato, PAN, un compuesto tóxico).
La formación del HNO3 se produce al final del día por reacción del NO2 con radicales oxhidrilo:

Durante la noche los radicales OH· pueden reaccionar con el NO dando ácido nitroso, que se disocia en presencia de luz, pero es estable durante la noche.
OH· + NO → HONO
HONO + hν → OH· + NO
Durante la noche las reacciones de smog fotoquímico se ven muy reducidas al necesitar la luz para funcionar, aunque éstas pueden continuar a través de otros compuestos. [7]
Legislación aplicable
[editar]La Unión Europea ha aprobado la Directiva sobre los COVs "Directiva del Consejo relativa a la limitación de las emisiones de compuestos orgánicos volátiles debidas al uso de disolventes orgánicos en determinadas actividades e instalaciones". El objeto de esta Directiva es prevenir y minimizar los efectos directos e indirectos de las emisiones de compuestos orgánicos volátiles al medio ambiente, principalmente a la atmósfera, y los riesgos potenciales para la Salud Humana, por medio de medidas y procedimientos que deben implementarse en las actividades definidas en su Anexo I.
- Directiva 96/61/CE relativa a la prevención y al control integrados de la contaminación (IPPC) que establece un sistema de autorizaciones para actividades industriales tomando en cuenta determinadas sustancias contaminantes sobre las que fijará valores límite de emisión para concesión del correspondiente permiso. Uno de los compuestos a tener en cuenta es el de los órgano volátiles o metales y sus compuestos. En octubre de 1999 se deberá transponer en el Estado español.
- Directiva 76/769 relativa a la aproximación de las disposiciones legales reglamentarias y administrativas de los estados miembros que limitan la comercialización y el uso de determinadas sustancias y preparados peligrosos.
- Directiva 67/548 relativa a la aproximación de las disposiciones legales, reglamentarias y administrativas en materia de clasificación, embalaje y etiquetado de las sustancias peligrosas.
- Directiva 92/72/CEE sobre la contaminación atmosférica por ozono troposférico.
- Real Decreto 1494 de setiembre de 1995 que desarrolla la anterior directiva en España.
- Ley de prevención de relaciones laborales sobre manipulación de sustancias peligrosas.
- Ley 10/1998 sobre residuos.
- Real Decreto 833/1998 por que se modifica lo relativo al Reglamento sobre residuos tóxicos y peligrosos.
- Ley 11/1997 de Envases y Residuos de Envases, de 24 de abril.
- Real Decreto 149/1989 sobre clasificación, envasado y etiquetado de pinturas y productos afines.
- Real Decreto 150/1989 sobre clasificación , envasado y etiquetado de disolventes.
- Real Decreto 74/1992 por que se aprueba el reglamento nacional de transporte de mercancías peligrosas por carretera.
- Real Decreto 2216/1985 Reglamento sobre declaración de sustancias nuevas y clasificación, envasado y etiquetado de sustancias peligrosas.[8]
Verdor
[editar]En la utilización de disolventes no solo se evalúa la toxicidad, sino también se establecen propiedades de su verdor, como es:
- Energía de evaporación, presurización, agitación entre otros.
- Reciclado.
- Solubilidad del soluto.
- Toxicidad atómica del proceso.
- Separación de los productos.
- Posible influencia en el producto/empaquetado.
Conclusión
[editar]Es importante para las industrias contar con formas adecuadas que permitan la comparación cuantitativa entre dos o más procesos o productos en los que se refiere a su impacto ambiental. Aparte de las cuestiones de balance económico y de sensibilidad social, la evaluación de la cantidad de residuos que genera y de su peligrosidad, es decir, de su capacidad nociva, requiere disponer de parámetros para la diversas formas de toxicidad, y eco-toxicidad, influencia en el calentamiento global, la capa de ozono estratosférico, la generación de ozono troposférico, riesgo de inflamación, etc.
Valorando la sustitución de los disolventes orgánicos clásicos por otros de origen renovable, que superen los riesgos y la contaminación.
Referencias
[editar]Bibliografía
[editar]- R. Mestres, Química Sostenible, Editorial Síntesis,(2011). 105–143.
- Disolventes y métodos de reacción no convencionales. ( Máster en Química Sostenible año 2012-2013 de la Universidad de Zaragoza)
- Wj. Crinnion, et al. (2010): The CDC fourth national report on human exposure to environmental chemicals: what it tells us about our toxic burden and how it assist environmental medicine physicians. Altern Med Rev,15(2):101-9.
- P.H. Howard, et al, Handbook of Environmental Degradation Rates, Lewis, 1991.
- M.C Mancheño, et al, Exposición Laboral a Disolventes, Unión Sindical de Madrid Región de CCOO, 2008.
