Wikichicos/Química/La materia

La materia o sustancia es todo aquello que tiene masa y conserva un lugar en el espacio, es decir, todo lo que nos rodea: la tierra, el agua, el aire, las nubes, las plantas.... Está formada por partículas muy pequeñas llamadas átomos.
Los átomos
[editar]
Los átomos son muy pequeños y no los podemos ver a simple vista. Tan pequeños que si tomamos una bolita de plastilina lo más pequeña que podamos en ella habría millones de átomos.
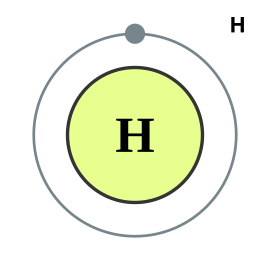
Las partes principales del átomo son las siguientes:[1]
- Núcleo: es el lugar ocupado por las partículas más pequeñas que el átomo que son los neutrones y los protones
- Neutrones. Tienen masa pero no carga eléctrica.
- Protones. Poseen carga eléctrica positiva (+). Tienen masa y es muy difícil que salgan del núcleo del átomo.
- Electrones. Poseen carga eléctrica negativa (-) y se desplazan en una órbita elíptica alrededor del núcleo del átomo. Tienen una masa muy pequeña.
- Órbitas. Caminos simulados que recorren los electrones al desplazarse alrededor del núcleo
Iones
[editar]

El número de protones (carga positiva) y electrones (carga negativa) en un átomo es el mismo, por lo que las cargas se equilibran a cero, es decir el átomo en estado normal es eléctricamente neutro. Sin embargo, los iones tienen un número de electrones diferente al de protones, por lo que tienen una carga positiva o negativa.
Un ión es un un átomo o molécula cargada eléctricamente y que por lo tanto no es eléctricamente neutro. Esto se puede entender como que, a partir de un estado neutro de un átomo o molécula, se han ganado o perdido electrones; este fenómeno se conoce como ionización.
Cuando un átomo pierde o gana electrones se transforma en un ion y lleva carga eléctrica. Como el electrón tiene carga negativa, cuando se añaden uno o más electrones a un átomo eléctricamente neutro, se forma un ion cargado negativamente. Al perder electrones se produce un ion cargado positivamente. El número de protones no cambia cuando un átomo se convierte en un ion.
|
Por ejemplo el átomo de hidrógeno neutro tiene un protón en el núcleo y un electrón en la nube de electrones, pero si gana un electrón se convierte en un ión negativo y se representa como . En el caso del hidrógeno tendría un protón en el núcleo y dos electrones alrededor. Si pierde su único electrón se convierte en un ión positivo y se representa como .
|
|
Los iones positivos se llaman cationes y los iones negativos se llaman aniones. El número representa el número de electrones que le faltan o que tiene en demasía |
- Notaciones posibles de un ión
-
Anión (con el signo menos en este caso)
-
Anión bromo
-
Anión flúor
-
Catión calcio
-
Catión rubidio
- Notaciones posibles del anión cloro
- Notaciones posibles del catión sodio
Estados de la materia
[editar]La materia existe en tres formas, llamadas estados de la materia, que son: sólido, líquido y gaseoso.
| Estado | Ejemplo | Moléculas | Características |
|---|---|---|---|
| Sólido | hielo | Las moléculas están juntas, prácticamente no pueden moverse. | Por las características de las moléculas, un objeto sólido permanece con el mismo volumen y no cambia su forma. |
| Líquido | agua | Las moléculas continúan estando cerca pero no están unidas unas con otras. Se pueden mover. | Por las características de las moléculas, los líquidos pueden cambiar de forma y fluir, aunque al igual que un sólido, conserva el mismo volumen. |
| Gaseoso | vapor de agua | Las moléculas pueden moverse cerca o lejos unas de otras. | Por las características de las moléculas, un gas puede variar su volumen y tiende a rellenar el envase en el que está contenido. |

Moléculas
[editar]
Una molécula es la cantidad más pequeña que puede existir de una sustancia química. Si una molécula se dividiera en trozos más pequeños, sería una sustancia diferente.
Las moléculas están formadas por átomos unidos de una forma determinada. Por ejemplo, los átomos de oxígeno siempre tienen dos enlaces con otros átomos, los átomos de carbono siempre tienen cuatro enlaces con otros átomos y los átomos de nitrógeno siempre tienen tres enlaces con otros átomos.
En gases como el aire, las moléculas simplemente vuelan. En los líquidos, como el agua, las moléculas están pegadas, pero pueden moverse. En los sólidos, como el azúcar, las moléculas sólo pueden vibrar.
Fórmula química
[editar]
La fórmula indica qué átomos y cuántos de cada tipo hay en la molécula.
Las letra indica de qué elemento químico es cada átomo. Se llaman símbolos químicos y tienen una o dos letras.
Los subíndices son pequeños números situados en la parte inferior derecha de un símbolo. indican el número de cada tipo de átomo. Por ejemplo, el metano tiene un átomo de carbono (C) y cuatro átomos de hidrógeno (H); la fórmula química es CH4.
La molécula de azúcar glucosa tiene seis átomos de carbono, doce de hidrógeno y seis de oxígeno, por lo que su fórmula química es C6H12O6.
Las fórmulas químicas se utilizan en las ecuaciones químicas para describir las reacciones químicas.
Tipos de fórmulas
[editar]Hay tres tipos de fórmulas principales: fórmula molecular, fórmula estructural y fórmula tridimensional
- Fórmula molecular: indican simplemente los números de cada tipo de átomo en una molécula, sin información sobre la estructura. Por ejemplo, la fórmula molecular de la glucosa es (12 átomos de hidrógeno, 6 de carbono y 6 de oxígeno).
- Fórmula estructural: es una representación gráfica de la estructura molecular, que muestra cómo se ordenan o distribuyen espacialmente los átomos. Se muestran los enlaces químicos dentro de la molécula.
- Fórmula tridimensional: indica, además de los átomos que forman la molécula y los enlaces, la distribución de los átomos en el espacio.[2]
| Tipos de fórmulas | |||
|---|---|---|---|
| Compuesto | Fórmula molecular | Fórmula estructural | Fórmula tridimensional |
| Agua | H2O | 
| |
| Sal común (cloruro sódico) |
NaCl | NaCl | |
| Amoníaco | NH3 | 
|
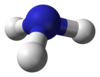
|
| Glucosa | C6H12O6 | 
|
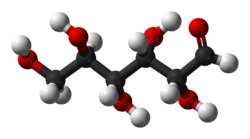
|
-----------------------------------------------------------------------------------------------------------------------------------------------------
Ejercicios
[editar]