Disolventes en la Industria Química/Clasificaciones de los disolventes según su peligrosidad
Los disolventes son muy comunes en muchos lugares de trabajo en los que los trabajadores se olvidan de lo peligrosos que pueden resultar. Se entiende por disolvente aquella sustancia, habitualmente líquida, que se utiliza para disolver otra sustancia. Aunque estos pueden utilizarse en ocasiones sin riesgo alguno, pueden provocar problemas de salud al contacto con la piel o al inhalar sus vapores. Otros de los riesgos son los vapores de muchos disolventes, que son inflamables y explosivos, e incluso muchos son dañinos para el medio ambiente.
Parámetros de peligrosidad en disolventes[editar]
Para determinar si un disolvente utilizado en la industria es peligroso, para la salud humana y medio ambiente, se han establecido unos parámetros que nos dan información acerca del peligro del uso de estas sustancias.
Los parámetros más importantes a la hora de etiquetar un producto químico según su peligrosidad son:
Punto de inflamación (Flash Point)[editar]
El punto de inflamación se corresponde con el Flash Point, que es la temperatura mínima necesaria para que un material inflamable desprenda vapores que, mezclados con el aire, se inflamen en presencia de una fuente ígnea, para volverse a extinguir rápidamente por sí sola una vez retirada la fuente de activación.
Este parámetro es mayor en sustancias con puntos de ebullición (Te) altos. Por ejemplo, se puede estimar de forma orientativa para hidrocarburos a partir del punto de ebullición (Te) mediante la siguiente fórmula[1]:
- ti = 0,683 Te -71,7
- ti = 0,683 Te -71,7
Respecto a la peligrosidad, no interesa que este parámetro sea bajo, ya que conlleva a una alta inflamabilidad.
| Disolvente | Flash Point (ºC) |
|---|---|
| Pentano | - 40 |
| Hexadecano | 126 |
| Decano | 46 |
| Benceno | -11 |
| Clorobenceno | 30 |
| Bromobenceno | 51 |
| Diclorometano | - |
| Triclorometano | - |
| Agua | - |
Temperatura de autoignición[editar]
Se denomina temperatura de autoignición a la temperatura mínima de un sustancia a la que puede arder en ausencia de una fuente de ignición, normalmente mediante contacto con una superficie caliente como lineas de vapor, tuberías de aceite, etcétera. A esta temperatura se alcanza la energía de activación suficiente para que se inicie la reacción de combustión.
Este parámetro recibe también el nombre de temperatura o punto de autoencendido, temperatura de ignición espontánea o autógena y hasta puede aparecer solamente como temperatura de ignición.
| Disolvente | Tª de autoignición (ºC) |
|---|---|
| Disulfuro de carbono | 90 |
| Eter dietílico | 160 |
| Acetaldehido | 175 |
| Heptano | 204 |
| Hexano | 225 |
| Alcohol etílico | 365 |
| Metanol | 385 |
| Acetona | 465 |
| Benceno | 560 |
| Diclorometano | 615 |
En general, los alcanos y los éteres presentan bajas temperaturas de autoignición, mientras que los compuestos halogenados presentan valores altos.
Límites de explosión[editar]
También llamados límites de explosividad, existen dos términos principales:
- Límite inferior de explosividad: Corresponde a la concentración de vapor en el “flash point”,es decir, el punto de inflamacion a la que la ignición conduce a una explosión.
- Límite superior de explosividad: Concentración de vapor que es demasiado rica para explotar, es decir, la máxima concentración del gas en el aire por encima de la cual una explosión no es posible.
Estos parámetros dependen de la concentración de oxígeno, concentración de gases distintos al oxígeno, tipo de gas inerte y concentración, tamaño del equipo, dirección de propagación y presión, temperatura y composición de la mezcla.
| Productos | Inferior | Superior |
|---|---|---|
| Hidrógeno | 4.1 | 74.2 |
| Metano | 5.3 | 13.9 |
| Acetileno | 2.5 | 80.0 |
| Etileno | 3.02 | 34.0 |
| Etano | 3.12 | 15.0 |
| Propano | 2.37 | 9.5 |
| n-butano | 1.6 | 8.5 |
| Pentano | 1.4 | 8.0 |
| Hexano | 1.25 | 6.9 |
| Ciclohexano | 1.31 | 8.35 |
| Benceno | 1.40 | 8.0 |
| Dietiléter | 1.9 | 36 |
Límites de explosividad (% Volumen en aire) Los éteres y alcoholes presentan amplios intervalos de explosión.
Formación de peróxidos[editar]
Los peróxidos son sustancias que presentan un enlace oxígeno-oxígeno y que contienen el oxígeno en estado de oxidación = −1. Por lo tanto, se comportarán habitualmente como sustancias oxidantes. En contacto con material combustible pueden provocar incendios o incluso explosiones.
Respecto a la formación de estos a partir de disolventes en la industria, un ejemplo son los éteres, que tienen grupos CH unidos al oxígeno que pueden formar hidroperóxidos. La reacción requiere oxígeno y se acelera por luz, catalizadores metálicos y aldehídos. En contacto con material combustible pueden provocar incendios o incluso explosiones, y por ello son tan peligrosos.
Los éteres se suelen almacenar sobre KOH, ya que destruye los peróxidos y actúa como desecante. Los éteres no suelen usarse a escala industrial por esta tendencia a explotar.
Daño inmediato y norma de exposición ocupacional[editar]
- Daño inmediato para la vida y la salud: Máxima concentración de vapor de la que una persona puede escapar en 30 minutos sin daño irreversible para su salud o sin efectos que le impidan escapar.
- Norma de exposición ocupacional: Exposición a un disolvente en el aire a las que no hay indicación de daños causados incluso tras exposiciones diarias en jornadas de 8 horas.
Toxicidad de los disolventes[editar]
La toxicidad es un término general que se refiere a cualquier efecto adverso o daño que es resultado de la exposición a una sustancia química o a cualquier otra sustancia. Puede considerarse como una propiedad molecular inherente e inalterable que depende de la estructura química, aunque también depende, en gran medida, del organismo con el que la sustancia entre en contacto.
Dentro de la familia de los disolventes se pueden establecer unas categorías según las características de toxicidad:
- Carcinógeno: Aquel que actúa sobre los tejidos vivos de tal forma que produce cáncer.
- Mutágeno: Agente físico, químico o biológico que altera o cambia la información genética (usualmente ADN) de un organismo y ello incrementa la frecuencia de mutaciones por encima del nivel natural.
Clasificaciones de peligrosidad[editar]
NFPA 704 (National Fire Protection Agency)[editar]
NFPA 704 es el código que explica el "diamante de materiales peligrosos" establecido por la Asociación Nacional de Protección contra el Fuego, utilizado para comunicar los riesgos de los materiales peligrosos. El rombo NFPA 704 nos permite identificar los riesgos asociados a los materiales peligrosos; fue diseñado para identificar materiales en almacenamientos, sin embargo, es también usado para contenedores durante el transporte.
Los aspectos más importantes en esta norma son los colores y números que se asignan para indicar el nivel de riesgo.
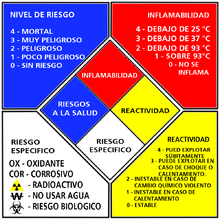
Las cuatro divisiones tienen colores asociados con un significado:
- Azul: Peligros para la salud.
- Rojo: Amenaza de inflamabilidad.
- Amarillo: Peligro por reactividad.
- Blanco: Indicaciones especiales para algunos materiales, indicando que son oxidantes, corrosivos, reactivos con agua o radiactivos.
Las divisiones azul, roja o amarilla tienen valores de 0 (sin peligro) a 4 (peligro máximo).
Glaxo - Smith - Kline[editar]
GlaxoSmithKline (GSK) es una empresa británica de productos farmacéuticos, productos de cuidado dental y de cuidado de la salud. Esta empresa es el resultado de la fusión de Glaxo Wellcome y SmithKline Beecham. A su vez, es una empresa de investigación bioquímica y sus productos abarcan una gran parte en el campo de la farmacia.
Esta empresa realizó una guía[2] sobre los diferentes disolventes que se utilizan en la industria química, clasificándolos según una serie de parámetros característicos de estas sustancias, entre los que se encuentran los descritos anteriormente al inicio del capítulo. Inicialmente, estaba formada por 47 sustancias, sin embargo, debido a las nuevas investigaciones y mayores conocimientos se ha incrementado el número hasta 110.
Se marcan los diferentes parámetros de peligrosidad asociados a cada disolvente y a un color en particular, estos colores indican la peligrosidad del disolvente conforme al parámetro indicado:<b
- Amarillo:Sustitución recomendada - No existen restricciones actualmente, pero en el futuro se deberían aplicar.
- Naranja: Sustitución recomendada - Se aplican restricciones de regulación.
- Rojo: Tiene que ser sustituido - Se aplica la prohibición.
Se puede observar que los disolventes más peligrosos según esta clasificación son:
- Triclorometano
- Cloroformo
- Dicloroetano
- 2- Metoxietanol
- Benceno
Estudiando los dos tipos de clasificaciones se puede observar que el gran trabajo realizado por GlaxoSmithKline nos deja una clasificación realmente amplia y muy detallada sobre una gran cantidad de disolventes, su riesgo y parámetros de peligrosidad, e incluso su impacto sobre el medio ambiente. La clasificación NFPA 704 se podría decir que es más sencilla, ya que contiene información más general con un número de parámetros menor, y a la vez más práctica en la mayor parte de las industrias.
Además de las clasificaciones explicadas anteriormente existen otras clasificaciones; por ejemplo, el Método EHS (Environmental Health and Safety) y el Método LCA (Life Cycle Assessment)
Referencias[editar]
- ↑ NTP 379: Productos inflamables: variación de los parámetros de peligrosidad. Instituto Nacional de Seguridad y Salud en el Trabajo http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/NTP/Ficheros/301a400/ntp_379.pdf
- ↑ GSK Solvent Selection Guide 2009 http://www.rsc.org/suppdata/gc/c0/c0gc00918k/c0gc00918k.pdf
Bibliografía[editar]
- Disolventes y métodos de reacción no convencionales. (Máster en Química Sostenible, año 2012-2013, Universidad de Zaragoza)
- " Handbook of Solvents". G. Wypych, Chemtech, 2001
- "Solvents and solvent effects in organic chemistry", C. Reichardt.
- "The properties of Solvents", Y. Marcus, Wiley, Volume 4", Universidad de Jerusalem, Israel.
- " Solvent - free organic synthesis", T. Koichi
